2018年8月31日/基因宝jiyinbao.com/—任何近期观看过哥伦比亚广播公司(CBS)网站上关于引发生物学医学研究变革的CRISPR基因编辑工具的 60分钟视频片段[1]的人都会得出结论:这种基因编辑技术正处于开发出一连串治愈方法的边缘。但是最近的一项研究[2]揭示出在部署这种著名的“分子剪刀”之后,一大堆染色体片段会发生缺失和重排。
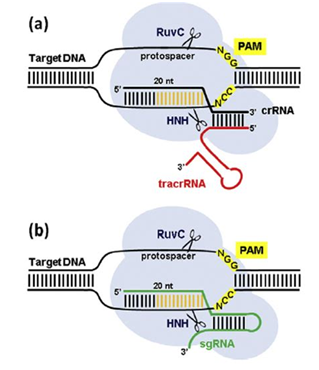
CRISPR是2012年发现的,它出色地让细菌抵抗病毒感染。这种“规律间隔性成簇短回文重复序列(clustered regularly interspaced short palindromic repeats, CRISPR)”是简单的DNA序列,在基因组中起着着陆带的作用,在那里,经过改造的“向导RNA(gRNA)”将一种酶运送到所需的基因上,对这个基因进行修饰或移除。当这种酶沿着双螺旋DNA进行切割时,天然的DNA修复随后发生。Cas9是一种经常使用的DNA切割酶。
图片来自Nature Biotechnology, doi:10.1038/nbt.4192。
与导入基因的常规基因疗法不同的是,CRISPR会在精确的位置上交换或移除基因。不过,在去年12月,美国食品药物管理局(FDA)花了27年的时间批准了首个基因疗法Luxturna用于治疗特定形式的遗传性失明。因此, CRISPR药物不会很快进入CVS(美国零售药店巨头)或沃尔格林(Walgreen, 美国医药零售巨头)的货架上。
在这项研究[2]中,来自英国威康基金会桑格研究所的研究人员并不是世界上首次报道CRISPR存在故障,而且肯定也不会是最后一次报道。
在对细胞开展的实验中,Allan Bradley、Michael Kosicki和Kärt Tomberg研究了CRISPR的预期着陆位点之外的基因组区域,就像是在已知存在拼写错误的书籍部分章节之外的其他章节中寻找错误。他们发现大量的DNA片段发生缺失、添加和翻转,而且一些DNA片段甚至从原始的位置上经移除后被插入到其他的DNA位置上。尽管“脱靶”效应是广为人所知的,而且关于CRISPR的小问题已被修复—更安全的酶、运送方法和检测工具,但是早期的研究可能只见树木不见森林。
这些研究人员没有使用过去研究中使用的DNA修复和染色体发生变化的癌细胞,而是靶向来自小鼠的干细胞和经过“永生化的”人视网膜细胞中的一个得到很好研究的基因。这两种细胞用于多种临床基因编辑应用中。
就像飞机坠入玉米田一样,CRISPR-Cas9在细胞内着陆,一次性吹走了数千个DNA碱基,最长的DNA片段有9500个碱基。这种损伤从靶位点上反射出来,引发染色体混乱,而单碱基突变(SNP)也出现,甚至出现在切割位点之外的区域上。通常,不止一件事情出了问题。这种损伤可能杀死细胞或者引发它发生癌变。
DNA片段缺失能够暴露隐性的基因变异;无论发生在什么地方,DNA片段插入和易位改变了基因控制。将一个基因移动到一个致癌基因附近的位点可能会产生第一次突变“命中”,当第二次突变发生时,这次突变命中会在生命后期引发癌症产生。这些研究人员猜测“在对数十亿个细胞进行编辑的临床环境下,产生的大量不同突变使得每个实验方案中的一个或多个经过编辑的细胞可能发生重大的致病性病变。”
这些实验存在着多种对照和复核:不同的递送方法(电穿孔而不是病毒载体);不同的靶基因;具有易于区分的染色体组的小鼠杂交品系,就像是将白色和黑色袜子放入干衣机中随后产生拼凑物;重复干预四次。这些研究人员总结道,“潜在的缺失结果的多样性是巨大的。”
事后影响?
经过编辑的基因组的这种不可预测的结果是否会减慢进入临床试验的轨迹,或者至少能够缓解炒作?人们对此存在着不同的观点。
作为美国北卡罗来纳大学和德克萨斯大学西南医学中心的一名基因治疗先驱,Steve Gray将CRISPR冲刺与基因疗法的马拉松比赛进行了对比。“据我所知,CRISPR涉及的明显且重要的安全问题尚未得到解决。这种技术是非常令人兴奋的,但是CRISPR可以从基因疗法的历史中了解到走得太快的后果,毕竟很多基础生物学特性和风险尚不完全清楚。”
Steve Gray将病毒载体比作为运送包裹的FedEx卡车。如果说传统的基因疗法运送包裹到建筑物中,那么基因编辑则将它传递到特定书桌中的特定抽屉里。
Gray开创性地开发出针对贝敦氏症(Batten disease)、雷特综合征(Rett syndrome)、戴萨克斯症(Tay-Sachs disease)、克拉伯氏病(Krabbe syndrome)和巨轴索神经病(giant axonal neuropathy)的基因疗法[3]。在1999年的一项临床试验中一个年龄18岁的人死亡和两年后的另一项试验中出现患上白血病的副作用后,基因疗法临床试验就停止了。
开发CRISPR的公司淡化这种技术的危险,指出断裂的染色体是DNA自然修复的一部分。Intellia治疗公司(Intellia Therapeutics)的 Jennifer Smoter解释道,“Intellia治疗公司不认为这些发现会显著影响基于CRISPR的疗法的前进之路。正常细胞中的DNA在没有其他的干预的情形下会持续地经历断裂、修复和其他的重排。在DNA断裂后发生大片段缺失在本领域中是已知的。分裂细胞(dividing cell)使用高保真修复:切除位于双链DNA断裂两侧的较长DNA片段,并且这些观察到的缺失可能来自于这个过程。”“采用任何基因组编辑技术或自然发生的断裂都会观察到这种”影响。也就是说,这个问题在于自然的DNA损伤/修复反应,而不是基因编辑工具。
Intellia治疗公司使用脂质纳米颗粒运送系统对一些单基因疾病和癌症进行了临床前研究。到目前为止,针对小鼠和猴子的实验没有显示出癌症的迹象,不过这家公司正在靶向肝细胞,而不是这些来自威康基金会桑格研究所的研究人员使用的快速发生分裂的细胞。Smoter补充道,细胞选择可能解释了较大的DNA片段缺失。
Editas医学公司(Editas Medicine)发言人Cristi Barnett回应道,“非预期的基因组变化(包括这些研究人员描述的那些变化)的产生适用于所有基因组医学方法,从基于慢病毒随机插入的方法,如用于CAR-T细胞疗法中使用的那些方法,到基因组切割方法,如锌指核酸酶(ZFN)、megaTAL核酸酶和CRISPR。”
Barnett补充道,该公司的临床前实验正在淘汰对细胞的治疗相关性产生不利影响的干预措施。“关于CRISPR的一个好处就是对它有如此多的兴趣,并且有很多人在研究它。但是,再一次地,在我们努力开发基于CRISPR的疗法的过程中,我们注意到但并没有特别关注这一最新的研究成果。”
对于非分裂细胞,CRISPR可能会更安全吗?
德克萨斯大学西南医学中心分子生物学教授Eric Olson认为如此。他的团队利用CRISPR和一种不同的辅助分子(即Cpf1)在小鼠体内和不能分裂的人心肌细胞中校正导致杜氏肌肉营养不良症的基因突变。“这项研究的结果不应该被过度解读。对破坏性的肌肉疾病而言,它是一种警示说明,但不是阻碍进展的障碍。”由于肌肉细胞不会分裂,它们不会变成癌细胞或传递受损的基因。
展望未来
如果有任何方法让CRISPR基因编辑进入临床的话,那么它有很多需要加以优化的变量。采取的策略就是使用不同的修复机制;运送途径;细胞类型;靶基因;分子剪刀和gRNA。
与哥伦比亚广播公司网站上的关于CRISPR的60分钟视频片段中的激情澎湃的非常炫丽的声明不同的是,ClinicalTrials.gov网站上关于利用CRISPR的疗法的名单仅有17个条,这是有些奇怪的。这个名单包括一个在无实体的内脏中开展的实验;研究镰状细胞病患儿的父母的“知识、态度和信仰”;遗传性麻醉不耐受的自然史研究,这都与基因编辑无关。大多数利用CRISPR的疗法来自中国。很明显,炒作远远超过现实。
关于CRISPR基因编辑未来的最后一句话来自1990年的French Anderson,他领导了第一个用于治疗遗传性免疫缺陷的基因治疗临床试验。
“CRISPR-Cas9的情况类似于许多新的颠覆性技术。最初由于新的可能性而引起人们巨大的兴奋。随后发现了有害的副作用,这种兴奋之情大幅下降。经过长时间的努力,这种技术的全部价值得到实现。这正是基因治疗经历的事情。CRISPR-Cas9是一种非常强大的技术,将在未来得到广泛使用。这种意想不到的基因组损伤只是一个亟待解决的问题。”
随着时间的推移和合适的分子工具出现,就像基因疗法一样,CRISPR将找到自己的方式进入临床治疗。(生物谷 Bioon.com)
资讯出处:
Is CRISPR Gene Editing Doomed, Even As Gene Therapy Enters the Clinic?
参考资料:
1.CRISPR gene editing toole revolutionizing biomedical research
2.Michael Kosicki, Kärt Tomberg & Allan Bradley. Repair of double-strand breaks induced by CRISPR–Cas9 leads to large deletions and complex rearrangements. Nature Biotechnology, 36:765–771 (2018), doi:10.1038/nbt.4192
3.Hannah’s Hero: Steve Gray and the GAN Trial
4.Yu Zhang1,2,3,*, Chengzu Long1,2,3,*,†,‡, Hui Li et al. CRISPR-Cpf1 correction of muscular dystrophy mutations in human cardiomyocytes and mice. Science Advances, 12 Apr 2017, doi:10.1126/sciadv.1602814

 基因君官网
基因君官网