
由传奇基因治疗先驱和宾夕法尼亚大学研究员詹姆斯·威尔逊(JamesWilson)共同创立,一家与宾大合作的生物技术公司ScoutBio刚刚筹集了2000万美元的B轮融资,以加强其针对常见宠物疾病的一次性基因疗法管线。
没错,ScoutBio正在使用一些熟悉的腺相关病毒(AAV)技术递送治疗性转基因,治疗慢性肾病、慢性疼痛和炎性皮肤病特应性皮炎等疾病,以求改革针对这些慢性疾病的宠物药物。
融资由DigitalisVentures的CompanionFund和RiverVestVenturePartners共同领导,新投资者GreenSpringAssociates以及现有投资者FrazierHealthcarePartners、AdageCapitalManagement和CorrelationVentures也参与其中。
ScoutBio已与宾大佩雷尔曼医学院的基因治疗项目(GTP)开展AAV动物健康研究与开发合作,该项目由Scout科学顾问和联合创始人詹姆斯·威尔逊博士领导。近三十年来,GTP一直是基因治疗研究和载体发现与开发的全球领导者。通过Scout和宾大之间的单独许可协议,Scout获得多个基于AAV的候选兽医产品和用于动物健康的相关AAV技术的独家权利。
“Scout的使命是利用基因疗法的进步,大幅提升目前依赖长期服用药物的多个兽医领域的护理标准,”ScoutBio首席执行官MarkHeffernan博士说。“我们的方法旨在通过一次性剂量持续有效的治疗来改善患者的治疗效果,同时满足市场对长效宠物药物的需求,以提高依从性和便利性。”
“仅在美国,就有9000万只狗和9400万只猫,这突显了新一代药物的机会,这些药物可以显着提高主要慢性病的护理标准。我们对Scout满足这一需求的战略印象深刻,并期待支持他们进入临床开发。”DigitalisVentures技术合作伙伴CindyCole博士说。
Scout最先进的治疗候选药物旨在为患有慢性肾病相关的贫血症的猫提供猫红细胞生成素(EPO)的长期表达。这种疾病导致生活质量的逐步恶化,尚无FDA批准的治疗,并且目前的护理标准具有严重的缺点。最近的研究显示,猫接受一次肌肉注射后,其红细胞计数(EPO生物标志物)在数月内均有显着增加,并为此项目启动了一项临床试点实地研究(clinicalpilotfieldstudy,动物健康关键研究之前的阶段)。
一项针对424名兽医的专有调查显示,在所有其他治疗方法中,超过90%的兽医会使用具有Scout目标特性的产品来治疗猫贫血,并称其最吸引人的特点是终身功效。
“GTP期待将其在AAV研发领域的长期领导地位延伸到宠物健康领域,以应对与频繁用药相关的依从性挑战,并提供解决慢性病的新方法,”宾大GTP的威尔逊博士说。“现在,成熟的基因治疗技术和动物健康方面的医疗需求已经融合在一起,我们相信Scout在这个交汇点和机遇上定位非常明确。”
宠物基因治疗这一概念听起来十分有趣,但它会起效吗?
价格方面?
要知道诺华曾表示,其脊髓性肌萎缩症(SMA)基因疗法Zolgensma定价为400-500万美元具有成本效益。
即使体重调整为猫或狗,这也是惊人的。当然,该行业将提高CMC并降低成本。但也有人对此持怀疑态度。
Scout相信它可以向大量的宠物主人推销基因疗法,每一剂将低于一百万美元。他们的市场调查显示,有一半的宠物主人会花1000美元来治疗他们的宠物;接近四分之一将高达5,000美元。
通过将制造基因疗法所带来的更高效率与潜在的数百万的大众市场相结合,Scout认为它可以治疗这些动物并从中赚钱。
此外,他们补充说,动物药物开发并不像人类研发那样昂贵。在基因治疗成本方面,也许他们正在做一些有助于其他领域的事情。(生物谷Bioon.com)

今日,美国行业领先的多平台基因疗法公司Rocket Pharma宣布与REGENXBIO达成了一项全球独家许可协议。Rocket将拥有使用REGENXBIO的专有NAV?技术平台的AAV9(腺相关病毒9)载体的权利,去研发和推广Danon病的基因疗法。Rocket公司同时拥有选择其它两种未公开的AAV载体治疗Danon病的的独家权力。
REGENXBIO的NAV技术平台,是一种独有的AAV基因递送平台,拥有100多种新型的AAV载体,如AAV7,AAV8,AAV9和AAVrh10等。源自细小病毒(parvovirus)家族的AAV,是一类单链DNA病毒,能以接近100%的成功率将基因插入19号染色体的特定位点,并具有非致病性(大多数人体内携带该无害病毒)。
Danon病是一种罕见的神经肌肉和心血管疾病。其特征是复杂的心肌病,骨骼肌病和轻度认知障碍。据估计,美国和欧盟的患病人数为15,000至30,000。Danon病是由编码溶酶体相关膜蛋白2(LAMP-2)的基因突变引起的,LAMP-2是自噬功能的重要介质。通过可变的剪接方式,LAMP2基因可产生三种不同的LAMP-2变体:LAMP-2A,LAMP-2B和LAMP-2C。其中发生在LAMP-2B上的功能障碍性突变与严重的心脏病特征相关。在患者20-30岁后,由Danon病引起的进行性心力衰竭往往是致命的,届时将需要心脏移植。然而,心脏移植也仍然不是治愈性疗法,目前尚无可针对Danon病的特定疗法。
Danon病是Rocket首个基于AAV的基因疗法项目。Rocket自身的多平台开发方法,应用慢病毒载体(LVV)和AAV基因疗法平台。目前,Rocket主要的临床阶段试验是治疗Fanconi贫血症(FA)。此外还在对丙酮酸激酶缺乏症(PKD),1型白细胞粘附缺陷病(LAD-I),以及婴儿恶性骨质疏松症(IMO)进行临床前研究。
Rocket总裁兼首席执行官Gaurav Shah博士说:“Rocket很高兴与REGENXBIO合作,推进我们第一个衍生自NAV技术平台的基因疗法产品,这将加强Rocket以疾病为中心的多平台开发方法的潜力,从而在不受载体类型限制的情况下,获得潜在的先发优势。Danon病代表着一个有未满足医疗需求的重要领域。有着被深入了解的疾病生物学背景以及来自患者深切的渴求,我们相信Danon病是基因疗法的理想目标,并期望明年能开始临床试验。”
REGENXBIO总裁兼首席执行官Kenneth T. Mills先生表示:“这一许可协议,进一步证实了REGENXBIO的NAV技术平台在治疗多样严重疾病方面的应用潜力。REGENXBIO很高兴能通过开发Danon病的基因疗法,开启与新兴罕见病基因治疗领域的领先公司Rocket的合作关系。”(生物谷Bioon.com)


孤独症(Autism spectrum disorder,ASD)是一种广泛的神经发育障碍疾病。典型的孤独症行为主要表现为社会交往障碍、言语和非言语交流缺陷、兴趣狭窄和重复刻板行为等临床特征。目前已成为世界上人数增长最快的严重性病症,发病率高达1/59。全基因组关联研究和大规模测序研究发现基因组中常见变异和罕见的新生突变(de novo variants)与ASD有关,而隐性突变在孤独症中的作用并不明确。
近日,波士顿儿童医院等机构的研究人员分析了来自美洲、欧洲和中东的2343名孤独症患者以及对照组5852名普通人的“全外显子组”数据,发现基因隐性突变引发孤独症的情形比人们原先认为的更常见,可能有3%到5%的病例与此有关,文章发表在Nature Genetics杂志。
研究人员在5%的患者中发现了双等位基因突变,即来自父母的两个拷贝均发生突变时,显着增加了患孤独症的风险。但是这样的病例中,女性患者仅占10%,也印证了孤独症的“女性保护效应”(女性的孤独症症发病率显着低于男性)。
孤独症的发病原因复杂,与遗传和环境等诸多因素有关。既往研究发现的相关基因突变大多数是患者的新生突变,并非来自父母遗传。该研究中发现的41个基因的隐性突变导致孤独症,其中33个基因此前从未被发现与孤独症有关,而且一部分只在单一病例中体现,其影响尚需进一步研究证实。(生物谷Bioon.com)

Catalent是一家总部位于美国新泽西州的合同研究组织(CRO),4月15日该公司宣布,将以12亿美元收购Paragon Bioservices,后者是一家领先的病毒载体开发和基因疗法制造公司,开发和制造用于基因治疗的病毒载体。腺相关病毒(AAV)是最常用的基因治疗递送载体,该公司在AAV载体方面拥有专业知识,在质粒和慢病毒载体GMP制造方面也拥有独特的能力。
Catalent的主席兼首席执行官John Chiminski表示,“Paragon在快速增长的基因治疗制造市场上拥有无与伦比的专业知识,这将是我们业务的一个变革性补充,将从根本上增强我们的生物制品业务和我们为客户提供的端到端集成生物制药解决方案。”据悉,Paragon在过去25年一直与全球最好的生物技术和制药公司合作,开发和制造基于其转化技术的产品,包括AAV和其他基因疗法、下一代疫苗、肿瘤免疫疗法(溶瘤病毒和CAR-T细胞疗法)、治疗蛋白和其他复杂生物制剂。
根据双方达成的协议,Paragon公司将继续在其总裁兼首席执行官Pete Buzy及其管理团队的领导下工作。Paragon目前拥有约380名员工,将纳入到Catalent公司。
Buzy表示,“现有的投资者——Newspring Health Capital和Camden Partners非常支持我们实现今天的目标。我们很高兴与业内领先的药物开发和制造合作伙伴携手合作。这笔交易将使我们能够实现下一个发展阶段,并为客户及其患者的利益扩展我们的能力和平台。”
据《华尔街日报》报道,Catalent在2018年的销售额约为25亿美元。该公司的首席执行官John Chiminsky一直致力于提高该公司在高增长市场(如基因和细胞疗法)中的能力,目前该公司在这方面还没有建立强大的业务能力。2018年,Catalent以9.5亿美元收购了美国印第安纳州布卢明顿的Cook Pharmica,该公司专长是制造复杂药物。同年,Catalent还收购了总部位于英国的Juniper Pharmaceuticals,以扩大其合同制造业务。
Catalent公司预计基因治疗市场在中期将以25%的速度持续增长,并预计Paragon近期内仅占其业务的一小部分,但随着时间的推移,将有意义地加速其收入和息税折旧及摊销前利润的增长。预计2019年,Paragon将带来2亿美元以上的收入。
就在不到一个月前,3月25日,赛默飞世尔科技(Thermo Fisher Scientific)以17亿美元现金收购了基因和细胞疗法制造商Brammer Bio,后者是一家专注于基因和细胞疗法病毒载体制造的合同开发和制造组织(CDMO)。
这两项收购都在强调基因和细胞疗法未来在生物制药行业中的重要性。根据最近的一份行业报告,目前有近300种基因疗法正在开发,用于治疗100多种疾病。
今年3月22日,蓝鸟生物(bluebird bio)宣布将在北卡罗来纳州达勒姆市开设新的基因治疗制造工厂。该工厂将为其基因和细胞疗法生产慢病毒载体,包括用于多发性骨髓瘤的BB2121和BB21217,以及可能用于输血依赖性β地中海贫血(TDT)和镰状细胞病的LentiGlobin。
但与蓝鸟生物不同的是,许多基因治疗公司会与CRO和CDMOS签订载体制造合同。在基因疗法中,载体通常是一种经过改造的病毒,含有人类DNA。这种病毒通常是AAV,病毒的DNA或RNA被去除,替换为将被插入患者基因组的基因。在治疗时,病毒被注射到患者体内,之后渗透到细胞中,并将治疗性DNA插入细胞中,并整合至基因组。(生物谷Bioon.com)

2018年11月27日/生物谷BIOON/—CRISPR基因组编辑技术有望导致基因工程和治疗发生“变革性飞跃”,它几乎影响到医学的每个领域。根据2018年11月发表在美国整形外科学会(American Society of Plastic Surgeon)官方期刊Plastic and Reconstructive Surgery上的一篇标题为“CRISPR Craft: DNA Editing the Reconstructive Ladder”的论文,所涉及的医学领域包括整形手术,这种基因组编辑技术有望在从预防颅面畸形到治疗性皮肤移植再到新型无排斥移植等方面取得潜在的进展。
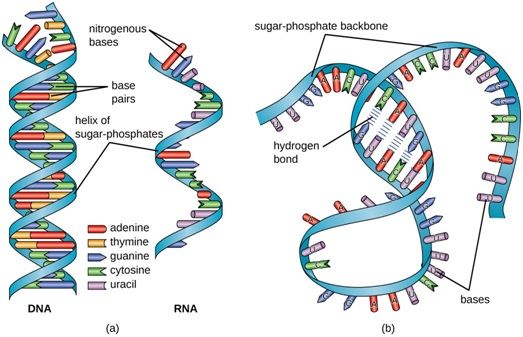
美国整形外科学会会员、麻省总医院外科医生Eric Chien-Wei Liao博士说,“CRISPR对治疗人类疾病的潜在影响包括对整形外科医生比较重要的几个领域,比如肿瘤学、伤口愈合、免疫学和颅面畸形。”在这篇关于再生医学的特稿论文中,Liao博士等人回顾了CRISPR基因组编辑的历史和机制,强调了它在整形手术(plastic surgery)和重建手术(reconstructive surgery)中的潜在用途和影响。
CRISPR对先天性畸形、伤口愈合和移植等有影响
人们最初发现CRISPR是细菌中的适应性免疫机制。在开发出CRISPR技术之前,开展基因编辑是费时费力的,仅限于具有先进分子生物学工具的实验室。
Liao博士等人写道,“鉴于CRISPR基因编辑具有简单性、特异性、高效性、低成本和多功能性等优点,它正在引发治疗潜力变革。CRISPR的潜在应用很多,肯定将会给整形手术和重建手术带来影响。”
Liao博士等人讨论了CRSIPR对整形手术具有可预见影响的一些关键领域,包括:
(1)颅面畸形(Craniofacial Malformations)。使用CRISPR技术的基础科学研究已引发了对颅面发育途径的新见解。CRISPR能够让人快速地鉴定出单个基因突变,并且可能有朝一日能够校正突变和阻止唇裂、腭裂和其他先天性畸形产生。
(2)伤口愈合和组织修复。基因疗法是一种增强伤口和组织愈合的有前景的方法。除了加快皮肤伤口愈合外,CRISPR还可能为骨骼、软骨、神经和肌肉的修复和再生提供新方法。
(3)细胞疗法和组织工程。遗传技术可能能够产生患者自身(自体)细胞或者对它们进行修饰,从而能够用于移植或替换受损组织、刺激细胞发育或调节免疫功能。Liao博士等人写道,“产生具有治疗潜力的皮肤移植物的[技术]将在重建手术中产生广泛的影响。”
(4)皮瓣生物学和移植。除了对组织瓣进行修饰外,CRISPR基因编辑可能能够重编程血管化复合同种异体移植物(vascularized composite allotransplant)—比如,面部或手部移植物—来促进耐受性和阻止受者免疫系统引发的免疫排斥。类似的免疫调节方法也可能促进对动物供者组织产生耐受性(异种移植)。
Liao博士等人强调在利用CRISPR基因编辑实现这些临床进展和其他临床进展方面仍存在许多挑战,包括潜在的“脱靶”效应,美国食品药物管理局(FDA)监管和高成本,以及与对人类细胞和组织进行基因编辑相关的伦理问题。他们写道,“美国整形外科学会及其成员也应该成为利益相关者,并在未来参与讨论利用CRISPR改善我们的患者的伦理问题。”(生物谷 Bioon.com)
参考资料:
Danny S. Roh; Edward B.-H. Li; Eric C. Liao. CRISPR Craft: DNA Editing the Reconstructive Ladder. Plastic and Reconstructive Surgery, November 2018, 142(5):1355–1364, doi:10.1097/PRS.0000000000004863.