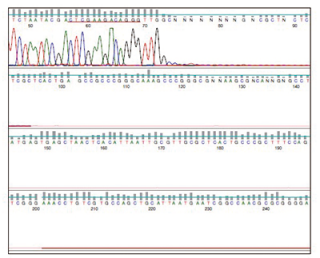
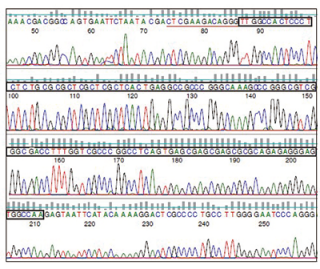
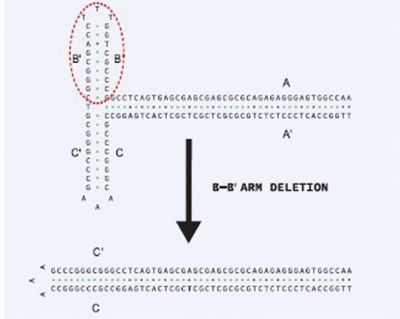
2019年7月21日讯/生物谷BIOON/—在一项新的研究中,来自美国波士顿儿童医院的研究人员报道了在遗传性心律失常小鼠模型中利用基因疗法抑制了这种疾病。这些发现为开发治疗遗传性心律失常的单剂量基因疗法提供了可能,而且也可能为治疗更为常见的心律失常(比如心房颤动)的单剂量基因疗法提供了可能。相关研究结果近期发表在Circulation期刊上,论文标题为“Gene Therapy for Catecholaminergic Polymorphic Ventricular Tachycardia by Inhibition of Ca2+/Calmodulin-Dependent Kinase II”。

参与这项研究的波士顿儿童医院遗传性心律失常项目主治心脏病学家Vassilios Bezzerides博士说道,“我们希望能够提供长期发挥作用的单剂量基因疗法。我们的研究为开发治疗遗传性心律失常的可转化基因治疗策略提供了概念验证。”
这项研究着重关注儿茶酚胺能多形性室性心动过速(CPVT),这是儿童和年轻人猝死的主要原因。这种心律失常通常由运动或精神压力引发,并且在平均12岁时首次出现,通常是突然失去意识。
当前的治疗方法包括β受体阻滞剂和氟卡尼等药物,手术可以阻断心脏左侧的神经,植入式心律复律除颤器(在CPVT中,这可导致中危及生命的并发症),以及让孩子尽可能少运动。
Bezzerides说道,“对于CPVT的治疗目前还不够:尽管接受治疗,25%至30%的患者仍会出现危及生命的心律失常。”
这些研究人员发现在健康的心脏组织中,一种称为CaM激酶(CaMKII)的酶可化学修饰RYR2,从而触发心肌细胞释放出更多的钙离子。在CPVT细胞中,这种修饰与遗传性的RYR2突变结合在一起,导致细胞中出现过量的钙离子水平,从而引起心律失常。
当这些研究人员阻断CaMKII修饰时,他们消除了这种组织模型中的心律失常。当用肽AIP(一种有效的选择性CaMKII抑制剂)阻断CaMKII本身时,他们获得了相同的效果。
利用基因疗法抑制CaMKII
鉴于CaMKII酶作用于心脏旁边的许多组织—并且是大脑中的记忆形成所必需的,这些研究人员希望能够特异性地抑制心脏中的CaMKII。他们在CPVT小鼠模型中测试了这种基因疗法。
他们设计了一种特殊病毒,当被注射到CPVT小鼠模型体内时,这种病毒选择性地移植到心脏并递送肽AIP。测试结果表明,AIP在大约50%的心脏细胞中表达,足以抑制心律失常,但在包括大脑在内的非心脏组织中无明显表达。
这些研究人员如今计划优化他们的基因治疗策略以便在大型动物模型中对它进行测试,并最终希望在CPVT患者中进行临床测试,这可能需要与其他医疗中心的合作。
治疗心脏病的通用方法?
Bezzerides和Pu认为这种基因疗法对于由各种RYR2突变引起的CPVT患者可能是有效的(已报道了160多种RYR2突变)。他们相信他们抑制心脏中CaMKII的整体策略可能有助于治疗更常见的心脏病。
Pu说道,“正常的心脏功能不需要CaMKII,但它会在许多形式的心脏病中被激活。在许多形式的心脏病(比如缺血性心肌病,心房颤动,肥厚性心肌病)的小鼠模型中,慢性CaMKII激活是有害的。我们的抑制CaMKII的基因疗法可能有助于改善这些其他心脏病类型的预后。”(生物谷 Bioon.com)
参考资料:
Vassilios J. Bezzerides et al. Gene Therapy for Catecholaminergic Polymorphic Ventricular Tachycardia by Inhibition of Ca2+/Calmodulin-Dependent Kinase II. Circulation, 2019, doi:10.1161/CIRCULATIONAHA.118.038514.

从中国科学院昆明动物研究所获悉,近期,该所科研人员完成了新版的树鼩基因组高精度测序、组装和注释。新版树鼩基因组填补了第一版基因组中约73%的拼装缺口。
据介绍,树鼩是一种与实验大鼠差不多大小的小型哺乳动物,为灵长类动物的近亲,在生物医学研究中颇具潜力。目前,树鼩已被用于感染性疾病如乙型肝炎、丙型肝炎、疱疹病毒感染、禽流感病毒感染等模型创建,在视觉系统研究、近视模型,以及一些肿瘤模型构建方面,显示了很好的前景。
2013年,为了解决树鼩用于疾病动物模型创建时缺少基因组学等遗传信息的问题,中国科学院昆明动物研究所姚永刚课题组牵头组织中科院动物模型与人类疾病机理重点实验室相关研究团队,联合华大基因,发表了利用二代测序技术测定的中缅树鼩的全基因组,较为全面地获取了树鼩的遗传特性,证实树鼩与灵长类动物的亲缘关系最近。基于此版树鼩基因组数据,姚永刚课题组建立了首个树鼩基因组数据库,实现了树鼩基因组数据的自由访问和共享。但由于二代测序读长过短等技术局限,第一版树鼩基因组中存在一些问题。
近期,来自姚永刚课题组的博士范宇利用单分子实时测序技术,结合高通量染色质构象捕获技术测序数据,完成了新版的树鼩基因组高精度测序、组装和注释。这一版树鼩基因组填补了第一版基因组中约73%的拼装缺口(163,220个),其中处于基因编码区的缺口全部得到填补。此外,新版树鼩基因组中,蛋白编码基因的数量与序列长度较第一版基因组有明显的质量提升,基因结构的精确度也明显上升。
基于第二版基因组信息,范宇等人完成了基因组重复序列的分析,发现120多个长转座子和400多万个包含短重复序列(长度小于150bp)和长重复序列(长度大于5kb)的卫星区域。对LINE1的分析发现,树鼩基因组中的LINE1占基因组的18.54%,这种基因组占比和人类的类似。与包括人类、猕猴和小鼠的基因组结构变异对比分析后发现,相比较于人类,树鼩基因组中含有221个结构变异,猕猴基因组中有188个结构变异,而小鼠基因组中的结构变异多达387个。有趣的是,一些结构变异,如位于MYSM1基因和SLC35D1基因间的区域,只出现在树鼩和灵长类动物中,这一结果也从结构变异的角度说明,相比于小鼠,树鼩与灵长类动物在基因组方面有更高的相似性。
据悉,为了更好地展示最新版的树鼩基因组信息,课题组将新版基因组数据、注释信息、群体遗传学参数、预测的基因共表达网络等数据,增加或更新在第二版树鼩基因组数据库中。这些用户友好型的数据库构建与更新,将为树鼩动物模型的研究提供相关基础数据,有望继续惠及树鼩研究领域。
上述研究工作以“Chromosomal level assembly and population sequencing of the Chinese tree shrew genome”为题,发表在动物学领域SCI期刊《Zoological Research》上。该研究工作得到国家自然科学基金委、中国科学院和云南省的资助。(生物谷Bioon.com)

近日,南非医学研究理事会(SAMRC)基因组学中心在开普敦正式启用,成为非洲首个高通量基因组测序中心。
南非医学研究理事会(SAMRC)成立于1969年,是南非卫生部下属机构,旨在通过研发和技术转移,改善南非人口健康,使民众能够享受到更好的生活质量。SAMRC主要研究领域包括结核病、艾滋病、心血管病及其他非传染性疾病、性别与健康、酒精及药物滥用等。
SAMRC基因组学中心是中南卫生领域合作的一项重要内容。2017年4月中非部长级医药卫生合作会议召开期间,SAMRC与深圳华大基因科技有限公司(简称华大基因)签署了合作谅解备忘录。2018年2月,双方正式签署合作协议,拟由华大基因提供设备和技术支撑,与SAMRC合作建设高通量基因组测序中心。一年多来,在两国政府部门的大力支持下,双方密切合作,通力配合,工作进展顺利。目前,约320平米的实验室改造完成,首套价值55万美元的华大基因测序仪已入驻实验室并完成组装测试。首批4名SAMRC技术人员已赴华大基因总部完成技术培训。华大基因还将派技术人员来南进行一年现场指导。
SAMRC主席兼CEO Glenda Gray教授表示,SAMRC基因组学中心将提升对人类全基因组测序、分析和数据存储的能力,使南非有机会进入医学研究的新时代。在SAMRC成立50周年之际,该中心的启用对其迈上前沿高水平研究新台阶具有重要意义。 (生物谷Bioon.com)

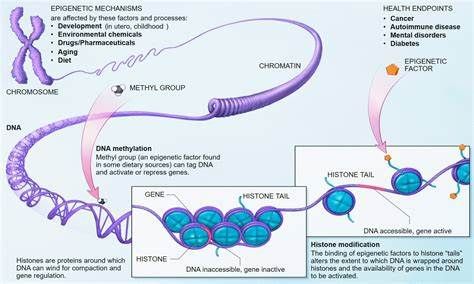
今日,Axovant Gene Therapies公司在第27届欧洲基因和细胞疗法协会(European Society of Gene and Cell Therapy)年会上宣布,初步临床数据表明,基因疗法AXO-AAV-GM2具有缓解戴萨克斯症(Tay-Sachs Disease,TSD)儿童患者疾病进展的潜力。AXO-AAV-GM2不但使TSD儿童患者达到正常发育里程碑,还改善了患者脑部的髓鞘形成。
TSD又称为GM2神经节苷脂病,是由HEXA和HEXB基因上的突变造成。这些突变使酶蛋白功能受损,进而导致有毒神经节苷脂在中枢神经系统中积累。患者因此出现神经退行性病变,认知障碍,瘫痪和早夭。这种致命的儿童溶酶体贮积病患者的平均预期寿命只有3-4年。目前,没有能够改变疾病进展的疗法出现。
Axovant公司的AXO-AAV-GM2基因疗法旨在将编码正常功能酶蛋白的基因分别使用AAV9和AAVrh8病毒载体导入患者体内,改善他们的生存并让儿童达到关键性发育里程碑。在临床前动物实验中,该基因疗法能够剂量依赖性提高酶活性,降低神经节苷脂的沉积,并且提高动物的生存期。
现有的临床初步数据来自两名TSD儿童患者。第一名晚期TSD患者在接受基因疗法后的第三个月至第六个月,脑脊液(CSF)中的Hex A酶活性较基线时增加了3倍。在第六个月时,与基线相比,使用CHOP-INTEND评估方法检测的运动能力评分从14分提升至18分,并维持在这一水平。
第二名儿童患者在接受基因疗法后的第三个月时达到正常的发育里程碑,且患者神经系统检查一切正常。经MRI检测,患者脑部结构正常,并有与该年龄正常脑部发育一致的髓鞘形成。患者的Hex A酶活性较基线时也得到改善,增加至正常酶活性的1.8%(预期酶活性超过正常酶活性的0.5%时会带来具有临床意义的效果)。CHOP-INTEND评分与基线相比,从58分提升至60分,并维持在这一水平。两名患者接受基因疗法后病情保持稳定。此外,AXO-AAV-GM2还显示出良好的安全性和耐受性。
“髓鞘的形成是健康儿童大脑发育的重要组成部分,但在TSD儿童患者中通常是异常的,”Axovant公司首席开发官Gavin Corcoran博士说:“我们很开心可以看到10个月大患者的髓鞘形成和神经肌肉的稳定性得到改善。”(生物谷Bioon.com)
小编推荐会议 2019无锡国际生物医药论坛暨第九届Cell Death & Disease国际研讨会-新药研发

自1990年全球首例基因治疗临床试验的成功开展揭开了基因治疗时代的序幕之后,病毒载体的安全性问题却接连出现,导致绝大多数基因治疗临床试验的中止。由病毒载体带来的致病风险成为阻碍基因治疗发展的严峻问题,开发更加安全有效并能高效表达的载体成为基因治疗研究的关键。
一、基因治疗常用载体概况
目前,基因治疗主要采用病毒和非病毒两种载体形式。从长远看,非病毒载体具有低免疫原型、低成本、易规模化等优点,因而具有更好的临床应用前景,但还存在较多未解决的问题,如转染效率、细胞毒性、靶向性等,因此当前大部分细胞和基因治疗项目所采用的载体都为病毒载体,使用非病毒载体的项目大约仅占项目总数的36.6%。
改造后的病毒载体去除了病毒本身的致病作用,但保留了病毒的包壳以及在细胞中进行复制或整合的功能蛋白,可通过基因重组技术与编码基因进行组装,然后感染细胞以达到治疗目的。
目前最为常用的病毒载体包括腺相关病毒(Adeno-associated virus,AAV)、慢病毒(Lentivirus,LV)、腺病毒(Adenovirus,AdV)和逆转录病毒(Retrovirus,RV)等,其他还有单纯疱疹病毒载体、豆苗病毒载体、溶瘤病毒载体等;非病毒载体主要包括脂质体、质粒等。
二、国内外基因载体CDMO平台
载体的构建包装和生产,在基因治疗产业链中处于中游。由于病毒载体的制造过程复杂、成本高昂,在技术水平上也要求更高的专业性,因此具有较高的准入门槛,市场格局较为稳定。
在这样的背景下,具有较强专业性、可以为病毒载体产品提供GMP生产资源的CDMO公司蓬勃发展起来,包括诺华、凯特这样的制药巨头,也纷纷将慢病毒和逆转录病毒载体的生产转向CDMO。
(一)全球病毒载体CDMO代表性公司
主要有Oxford BioMedica、Brammer Bio、Apceth、FujifilmDiosynth Biotechnologies、Lonza、Novasep、VGXI等。
1. Oxford BioMedica
作为慢病毒载体基因治疗的先驱,英国Oxford BioMedica公司是诺华的CAR-T产品Kymriah生产慢病毒载体的唯一供应商。此外,凭借其LentiVector?慢病毒载体递送技术,公司还与赛诺菲、GSK等制药巨头保持着合作关系,为他们提供工艺开发和生物加工等服务。
2. Brammer Bio
作为一家病毒载体CDMO公司,Brammer Bio为开发基因疗法和基因修饰细胞疗法的制药公司提供外包研究和制药服务。2019年3月,该公司被赛默飞世尔以17亿美元收购。
(二)国内病毒载体CDMO公司
目前,国内市场的行业集中度较低,且多数公司规模较小,技术和工艺水平有限,能够提供病毒载体产业化的企业较少,代表公司有和元上海、吉凯基因、汉恒生物、北京五加和等。
1. 北京五加和
北京五加和是专业从事基因治疗药物核心技术研发和服务的生物高科技公司,其基因治疗CDMO平台服务范围包括科研服务、符合GMP要求的中试和临床级制品的制备、质量研究服务,满足客户从早期研发、新药临床试验申报(pre-IND)和I/II期临床试验(IND)的要求。涉及的载体种类包括腺相关病毒载体(AAV)、腺病毒载体(AdV)、单纯疱疹病毒载体(HSV)、慢病毒载体(LV)和质粒DNA;全方位为基因治疗领域客户提供从工艺开发、小试、中试到临床样品生产的一体化CDMO解决方案,加速基因治疗或细胞治疗药物上市。
2. 和元上海
和元上海是一家集基础研究服务、基因治疗药物研发和临床级重组病毒产业化制备三大发展方向于一体的高新技术企业。和元拥有基因治疗载体研发中心、SPF级动物实验室、中试工艺开发与生产实验室,以及基于一次性技术的GMP级重组病毒车间,并依托先进的重组病毒产业化生产、病毒载体修饰改造与包装,CRISPR/Cas9基因编辑、脑立体定位注射及成瘤模型构建等多种技术,为基因治疗行业的崛起提供有力平台。
2019年3月5日,和元与GE医疗联手打造的基于一次性技术的病毒载体CDMO生产平台在上海张江正式开业运行,该平台是国内首个、近4500㎡基于一次性技术的GMP病毒生产平台,能够为基因治疗或细胞治疗相关药物研发提供GMP大规模生产一站式服务,生产一次就可以满足150名患者治疗所需药物载体量,一年能为2000名患者服务。
三、基因治疗领域重磅收购青睐AAV
近几年,基因治疗领域并购案例不断,大型制药企业收购在研发管线上拥有较强竞争力的创新公司,基因治疗领域在小型初创公司不断激增的同时,也逐渐向着稳定的市场格局发展。从被收购标的来看,AAV载体更受到收购方的青睐。
四、小结
纵观基因治疗的发展历史可以看到,基因疗法的发展必须要基于其在临床治疗方面的应用,因此,努力提高基因治疗的安全性和有效性是当前基因疗法发展的重中之重,其中尤以更安全高效的载体开发为最。未来,开发无细胞毒性、目的基因释放速度可控、可持续性作用及具备特异靶向性的新型载体,将是基因载体研究的方向。(生物谷Bioon.com)
2019年11月15日 讯 /生物谷BIOON/ –近日,一项刊登在国际杂志Nature Biotechnology上的研究报告中,来自北卡罗来纳大学Eshelman药学院等机构的科学家们通过研究开发了一种新方法,能够利用CRISPR基因编辑技术进行剂量依赖性的基因表达激活,文章中,研究人员描述了如何利用这种技术以一种可替换的方法来改变基因表达以及其工作的原理和机制。

图片来源:CC0 Public Domain
此前研究结果表明,CRISPR/Cas9基因编辑技术能抑制或激活基因的表达,但截至目前为止,其并不能用来促进剂量依赖性的基因表达激活;这项研究中,研究人员就发现了一种新方法,其能利用化学表观遗传修饰物(CEMs,chemical epigenetic modifiers),通过使用部分内源性染色质-激活器来激活所需的基因进行表达,这或许就能消除外源性转录激活剂的必要性。
研究者发现的新方法包括两种组分,其中第一种就是Cas9,其能与结合蛋白FKBP一起催化失活;第二种就是利用FK506制造的CEM,其能与特殊的分子相关联,而这种分子则能与所需的细胞表观遗传机器相互作用;具体地说,这种新方法能够制造激活CEM的分子,而该分子能帮助寻找基因激活机器,包括CEM114、CEM87和CEM88,诸如此类分子能与不同的酶类相结合,上述两个组分能被用来以研究者需要的方式激活基因的表达。
随后研究人员检测了这种新型系统,即利用绿色荧光蛋白感染HEK293T细胞,随后对表达导向RNA和非活性Cas9的细胞进行计数,紧接着研究者利用质粒表达和上述三种CEMs中的一种来检测基因表达的激活状况,他们必须等待两天才能够确认,是否与未处理的细胞相比绿色荧光蛋白的表达量会发生增加,研究者还仔细分析了用CEMs处理过的失活Cas9,来确定是否CEM系统能以一种所需的方式激活绿色荧光蛋白,在该过程中,研究者发现,使用CEM87进行处理是唯一能够增加绿色荧光蛋白表达的方法。最后研究者表示,这种新型技术能够用来在验证性研究中分析剂量依赖性的基因表达激活状况。(生物谷Bioon.com)
原始出处:
Anna M. Chiarella, Kyle V. Butler, Berkley E. Gryder, et al. Dose-dependent activation of gene expression is achieved using CRISPR and small molecules that recruit endogenous chromatin machinery, Nature Biotechnology (2019). DOI: 10.1038/s41587-019-0296-7