2019年8月17日讯/生物谷BIOON/—在一项新的临床研究中,一种可诱导的肿瘤定位基因疗法首次在胶质母细胞瘤患者中进行了测试。这种由两部分组成的方法涉及将一个编码免疫激活物的基因注射到脑瘤部位中并服用一种激活这个基因的药物,从而导致免疫激活物—白细胞介素12(IL-12)—的产生和免疫细胞渗入到肿瘤组织中。这些结果还提示着这种治疗可能延长患者的生存期。相关研究结果发表在2019年8月14日的Science Translational Medicine期刊上,论文标题为“Regulatable interleukin-12 gene therapy in patients with recurrent high-grade glioma: Results of a phase 1 trial”。
美国德克萨斯大学MD安德森癌症中心神经外科医生Frederick Lang(未参与这项新的研究)说,“所有近期的证据都提示着如果你能真正让免疫系统攻击肿瘤,那么你就有增加治愈肿瘤的潜力,而且这项[研究]正朝着这个方向发展。我认为这是令人兴奋的。”
胶质母细胞瘤是一种侵袭性和致命性的脑癌形式,在确诊后仅有6至9个月的平均生存期。领导这项研究的哈佛医学院神经外科医生Antonio Chiocca说,即使采用标准治疗(手术切除全部或部分肿瘤,然后进行6周化放疗),“平均7个月内. . .肿瘤复发了”。
许多因素使得胶质母细胞瘤成为一种令人生畏的疾病。首先,血脑屏障阻止许多化疗药物到达肿瘤。这种癌症本身是高度异质的,因此即使药物对某些细胞有效,其他细胞可能生长并取代它们。此外,Chiocca说,众所周知,胶质母细胞瘤是“免疫学冷性的”,这意味着它们会产生免疫抑制环境来限制抗肿瘤免疫细胞的浸润。Lang说,“将这种冷肿瘤变成热肿瘤是新型治疗方法的策略之一”。
为了在胶质母细胞瘤患者中做到这一点,这些研究人员给这些患者提供了IL-12蛋白,Chiocca将这种蛋白描述为一种“强大的免疫系统主调节剂”。但是,全身性IL-12治疗会产生毒性,引起流感样症状,或者在更严重的情形下,引起称为细胞因子释放综合征(cytokine release syndrome)的炎症反应,如果不加以纠正的话,这种炎症反应可导致器官衰竭。
为了最大限度地提高IL-12的局部水平,同时阻止危险的较高的全身性水平,Chiocca团队使用了一种编码IL-12基因的腺病毒载体并将它直接注射到肿瘤部位。为了控制IL-12剂量,这个基因的转录仅在对药物veledimex作出反应时才被激活。Chiocca解释道,“如果患者停止服用这种药物,这个基因会再次被关闭。”这种药物和病毒载体的所有权归属于Ziopharm肿瘤学公司(Ziopharm Oncology Inc.)。该公司与美国国家卫生研究院一起为这项临床试验赞助了资金。
药物veledimex可穿过血脑屏障,促进病毒载体中的IL-12表达,并且在携带胶质母细胞瘤的小鼠中缩小肿瘤。因此,Chiocca及其同事们在31名接受二次手术以切除再生的肿瘤组织的患者中测试了这种方法。
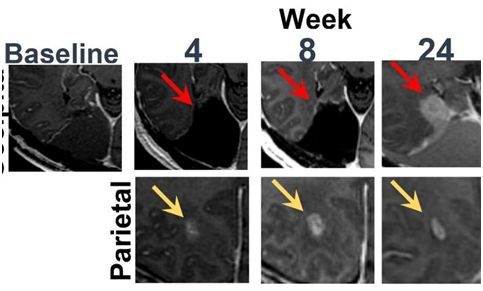
在手术期间,将这种病毒载体注射到已被切除的肿瘤周围的组织中。接着,这些患者服用不同的日剂量的veledimex(10、20、30和40毫克)长达两周。在服用veledimex之前、期间和之后,测量IL-12和γ干扰素—一种响应于IL-12而产生的细胞因子—的水平,结果显示它们的水平随着治疗的开展而上升并且在治疗停止后下降,而且它们的水平主要与药物剂量相关。在从需要进一步手术的5名患者体内切除的肿瘤组织中,这些研究人员发现与先前移除的肿瘤组织相比,更多的免疫细胞浸润到肿瘤区域中。Lang说,IL-12、干扰素和免疫细胞浸润数据都表明这种方法确实可以激活这个基因并提高免疫力。
大约一半的患者在治疗后出现细胞因子释放综合征,因此停止了治疗。根据这种并发症出现的频率和严重程度,在结合这些患者的服用药物依从性和生存数据,这些研究人员确定了veledimex的最佳剂量为20 mg。这组患者术后平均存活期为12.7个月,其中26.7%的人和13.3%的人分别存活了18个月和24个月。
美国加州大学旧金山分校神经外科医生Mitchel Berger(未参与这项新的研究)表示,“我们对I期临床试验的生存数据并不感到兴奋。”他补充道,不过“当你考虑到复发性胶质母细胞瘤是一种致命性的疾病且通常仅1%或2%的患者存活两年的这一事实时,让中位总生存期到达12个月并且超过10%一点点的患者有24个月的生存期是相当不错的。这非常令人鼓舞。”
Lang说,“这为推进更大的临床试验奠定了坚实的基础。”(生物谷 Bioon.com)
参考资料:
1.E. Antonio Chiocca et al.
Regulatable interleukin-12 gene therapy in patients with recurrent high-grade glioma: Results of a phase 1 trial. Science Translational Medicine, 2019, doi:10.1126/scitranslmed.aaw5680.
2.Immune-Activating Gene Therapy for Gliobastoma
https://www.the-scientist.com/news-opinion/immune-activating-gene-therapy-for-gliobastoma-66273
3.First clinical trial of drug-inducible gene therapy yields encouraging preliminary results
https://medicalxpress.com/news/2019-08-clinical-trial-drug-inducible-gene-therapy.html
 基因君官网
基因君官网