

资讯出处:Regrowing damaged nerves hinges on shutting down key genes

12月24日,国际学术期刊《美国国家科学院院刊》(PNAS)在线发表了中国科学院上海巴斯德研究所江陆斌研究组题为Epigenetic editing by CRISPR/dCas9 in Plasmodium falciparum 的最新研究成果。
疟疾与艾滋病、结核病一起被列为全球三大传染性疾病。疟原虫是引起疟疾的真核病原微生物,其中恶性疟原虫的感染致死率最高。分子水平的遗传操作是研究恶性疟原虫病理学以及抗药机制的重要工具。然而,疟原虫中通过同源重组机制进行基因修饰的效率极低,而且恶性疟原虫缺乏可运行RNAi机制的关键原件,因而对疟原虫的研究急需发展一种高效简便的基因编辑工具。
Cas9的两个关键酶活位点被突变后的dCas9保留了结合DNA功能,但是失去了切割DNA的功能。将dCas9与一些表观遗传修饰因子相偶联,可以高效地对特定基因进行转录水平的调节。江陆斌研究团队利用CRISPR/dCas9系统,在恶性疟原虫中成功构建了基于表观遗传修饰的新型基因编辑工具。分别将dCas9与恶性疟原虫乙酰转移酶(PfGCN5)和去乙酰化酶 (PfSir2a)融合表达。在特异性sgRNA 的引导下,dCas9重组蛋白可以在靶基因的转录起始位点(TSS)附近特异性调节染色质组蛋白乙酰化修饰水平,从而控制该基因表达的沉默或激活。运用此新型CRISPR/dCas9技术,该团队分别对恶性疟原虫感染人体红细胞的两个关键基因PfRh4和PfEBA-175成功地进行了表达调控,并诱导出相应的感染表型的变化。在此基础上,该团队进一步鉴定出恶性疟原虫生长必需基因PfSET1参与调节恶性疟原虫红内期生长过程的分子基础。该研究成果为恶性疟原虫基因编辑提供了新的有效的遗传操作工具,为恶性疟原虫功能基因组学研究提供了强大的遗传操作系统。(生物谷Bioon.com)

云南素有动植物王国之称,鱼类资源尤其突出。鱇浪白鱼(Anabarilius grahami)是分布在全国第二大深水湖——云南抚仙湖流域的特有鱼类,也是“云南四大名鱼”之一。鱇浪白鱼有一系列独特的生物学特点被认为和抚仙湖的形成和演化过程密切相关,此外,抚仙湖周边传统的车水捕鱼文化、神奇的界鱼石传说等也使得该鱼具有独特的人文价值。历史上,该鱼一直都是抚仙湖主产经济鱼类,因味鲜肉美而名扬四海。然而,上个世纪末以来,由于过度捕捞,产卵场地破坏,外来引入种竞争等多种因素,鱇浪白鱼的种群数量锐减,一度成为中国物种红色名录易危物种。鱇浪白鱼是云贵高原湖泊中一种典型的“3E”鱼类,即具有濒危(Endangered)、特有(Endemic)和经济价值(Economic)三重特点。
中国科学院昆明动物研究所一直积极推动鱇浪白鱼这一“3E”物种的保护与可持续利用研究。2003年首次突破该物种的人工繁殖,使其种质资源得以保存,并随后推动了其野外种群恢复(人工增殖放流)和本土渔业的利用(人工养殖)。2016年起,在云南省科技厅科技创新强省计划(2016AB024)的主要支持下,昆明动物所杨君兴团队联合华大基因等开展了鱇浪白鱼全基因组测序分析工作。组装获得的该物种基因组大小为1.006Gb,共注释到25250个蛋白编码基因。基于组装注释的鱇浪白鱼全基因组,团队进一步开展了三个方面的进化遗传分析。首先,下载了现今公共数据库中18种鲤科鱼类的基因组或转录组数据,通过比对获得4580单拷贝同源基因,基于这些基因构建了首个基于组学数据规模的鲤科鱼类各亚科之间的系统发育关系。其次,构建了鱇浪白鱼的种群历史动态,发现其种群数量变化与抚仙湖湖泊形成演化的三个周期具有非常密切的联系。再次,基于组装的基因组,团队还开发获得了33836个微卫星位点。随机选取50个位点,经过三重筛选,最终选择11条对鱇浪白鱼4个种群进行了遗传多样性的初步评估。鱇浪白鱼全基因组测序和微卫星位点的开发为其后续科学研究、物种保护与开发利用提供了重要的基因资源。该研究于近日发表在Frontiers in Genetics 杂志上。(生物谷Bioon.com)
2019年1月27日/生物谷BIOON/—在一项新的研究中,来自冰岛基因解码公司(deCODE genetics)、冰岛大学和雷克雅未克大学的研究人员发布了首个使用全基因组序列数据开发出来的全分辨率人类基因组遗传图谱。
该图谱提供了迄今为止关于人类进化的两个关键驱动因素之间的位置、速率和关联性的最详细观察:重组(recombination)—在卵子和精子形成中发生的基因组重组;并且新发突变(de novo mutation)—在我们的每个基因组中出现了几十个通常很小的变异,而且我们没有从父母那里遗传这些变异。这些过程共同确保每个人都是我们物种的独特版本,不过新发突变也是儿童罕见疾病的主要原因。相关研究结果发表在2019年1月25日的Science期刊上,论文标题为“Characterizing mutagenic effects of recombination through a sequence-level genetic map”。
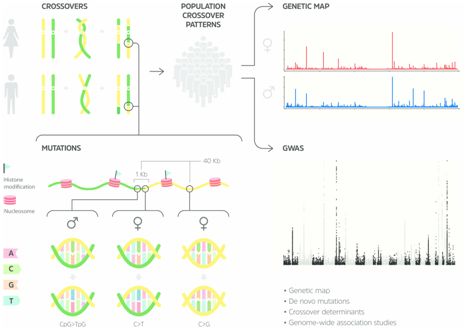
这篇论文介绍了冰岛基因解码公司利用冰岛独特的群体遗传资源构建出的最新基因组遗传图谱,并提供给科学界。2002年利用6000个微卫星标记发布的首个人类基因组遗传图谱有助于正确地组装第一个参考基因组。2010年,在推出第一台商业化全基因组测序仪的同时,冰岛基因解码公司使用了300000个微卫星标记来构建一个更加详细的人类基因组遗传图谱,用于指导对这种新型数据的分析。如今的这项新的研究利用了来自多代人的大约150000名冰岛人的序列数据,包括将近一半的人口,并且提供了450万次交叉重组和200000多个新发突变的精确定位。
论文共同通讯作者、冰岛基因解码公司首席执行官Kari Stefansson说,“在过去的20年里,我们一直致力于研究和发布新发突变和重组以及它们与人类进化和疾病的相关性。我们之所以这样做,既是因为更深入地了解作为一个物种我们是谁事关我们的根本利益,也是因为在冰岛,我们有独特的资源来解决这些问题以及它们与健康和医学的相关性。”
Stefansson博士总结道,“进化的经典前提是它首先由随机遗传变化驱动。但是,我们在这项新的研究中非常详细地观察到这个过程实际上是由基因组本身以及重组和新发突变之间存在关联性的事实系统地调节的。我们确定了影响重组率和位置的35个序列变异,并且显示在重组位点发生新发突变的可能性比基因组中其他位置高出50倍以上。此外,女性对重组的贡献更多,而男性对新发突变的贡献更大,并且新发突变构成了儿童时期罕见疾病的主要来源。我们在这项新的研究中观察到基因组是在一定范围内产生多样性的引擎。这显然有利于我们物种的成功,但对某些人来说,成本也很高,因此,我们必须努力解决罕见疾病,这是一项集体责任。”(生物谷 Bioon.com)
参考资料:
Bjarni V. Halldorsson et al. Characterizing mutagenic effects of recombination through a sequence-level genetic map. Science, 2019, doi:10.1126/science.aau1043.

2019年2月21日 讯 /生物谷BIOON/ –在即将步入婚姻殿堂之前,考虑未来伴侣的基因到底有多重要呢?基于许多机体特点背后的遗传因素如今已经被许多匹配网站所使用,而这看似也是符合逻辑的,比如机体的个性和同理心,其中很多因素被认为能促进特定夫妻间的机体原始化学反应和长期的潜力。因此,如今发展起来的结合基因检测和配对的网站也不足为奇。
图片来源:en.wikipedia.org
那么根据特定的基因来进行亲密伴侣的匹配是否有科学依据呢?有研究表明,分开抚养的同卵双胞胎对婚姻整体质量的评价是相似的,这就表明,基因对婚姻生活有着持久的影响,然而,与婚姻相关的特定基因目前研究人员并不清楚,其依然是个谜!
因此,根据基因特性的特定组合来预测人群婚姻的相容性往往是建立在薄弱科学研究基础上的,目前研究人员刚刚开始确定可能与婚姻幸福相关的基因以及这些基因是如何开始发挥作用的。
为何要研究基因对婚姻的影响效应?
作为一名临床心理学家,笔者非常感兴趣研究识别促进快乐婚姻的特殊因素,比如夫妻间如何处理争论?研究者希望能够阐明影响婚姻质量背后的遗传决定因素。笔者对催产素受体基因(OXTR)进行了研究,催产素,顾名思义“爱的荷尔蒙”,其在个体的情感依恋中扮演着关键角色;比如,催产素会在新生儿出生时大量涌入母体之中,同时其也会在性生活过程中激增;研究者推测,调节催产素的基因OXTR或许是在婚姻背景研究中的一个好基因,因为其常常控制着我们如何与他人产生联系;此外,OXTR也与一系列和人类社会行为相关的现象有关,包括信任和社交等。
研究者指出,OXTR基因与机体对社会支持所产生的生理学反应和特点有关,而这也对于支持过程非常重要,比如同理心;社会支持的质量是人群整体婚姻质量的一个主要决定因素,有证据表明,OXTR基因的突变可能会通过影响伴侣之间相互支持的方式从而与后来的婚姻质量联系起来。研究人员招募了79对已婚夫妇参与到了这项研究中,研究者要求每位伴侣找出一位与婚姻无关的重要个人问题,随后再与其伴侣讨论10分钟。在夫妇们完成调查问卷的同时,其每个人还提供了唾液样本,随后研究人员对唾液样本进行分析来确定其每个人携带OXTR等位基因的情况。

图片来源:en.wikipedia.org
基因突变和婚姻质量
基于此前的研究证据,研究人员重点对OXTR基因的两个特殊位点进行研究,这两个位点分别为rs1042778和rs4686302,正如预期那样,较高质量的社会支持与婚姻质量息息相关,此外,丈夫和妻子机体每个OXTR位点的基因突变与其在支持性讨论期间的行为有关。研究者发现,基因rs1042778位点处携带两个T等位基因拷贝的丈夫会认为其伴侣提供较低质量的支持,而这与其伴侣的支持技巧强弱并无关系。
携带TT基因型的丈夫往往更难将其妻子的行为解释为支持性的行为,这与其它的研究结果相一致,即暗示了同样的基因型在社会认知缺陷和自闭症中同样存在。值得注意的是,与携带不同等位基因组合的夫妇而言,携带相同等位基因的夫妇对婚姻的总体满意度较低;这就表明,若丈夫携带两个T等位基因的话,这种夫妇的情况可能更糟糕,部分原因是,这些男性很难将妻子的行为视为支持性的行为,而研究者们的统计学分析结果最终也支持了这一观点。

图片来源:en.wikipedia.org
现实意义
那么科学家们是否有必要开始筛查携带特定基因组合的丈夫,从而避免对婚姻有害的基因组合呢?笔者并不建议这样做,因为基因会影响机体一系列特性,有些可能会对婚姻的某些方面有害,但对于另一方面或许是有益的;尽管研究者发现,携带两个T等位基因似乎会成为社会支持背景下的一种负担,但探索性分析却发现,这种结合似乎也会对婚姻产生一种积极性的影响,但目前研究者并不清楚其背后所涉及的机制,研究者推测,对社会细微差别并不太敏感或许在婚期的其它方面会起到一定的保护作用,比如在出现分歧时能减少敌意的交流。
更重要的是,假设一个基因能够决定婚姻的成败,而这恰恰就低估了机体遗传因素和婚姻之间关系的复杂性了;有可能某些基因或多或少是有害的,而这取决于伴侣基因特性的其余部分。研究者指出,来自亲密伴侣的社会支持能减缓压力对机体身心健康带来的有害影响,在某种程度上,特定的基因型会削弱一个人获得支持的能力,这个人可能更容易受到压力的影响。因此,筛选OXTR基因上存在TT基因型的男性就能够帮助识别出存在压力相关问题风险的个体。
目前研究者还发现,OXTR基因上还要其它几个潜在的位点和其它基因或许与伴侣关系存在一定的相关性,后期他们还将进行更多的婚姻遗传学研究来探索基因和婚姻质量之间的密切关联。(生物谷Bioon.com)
参考资料:
【1】Henrik Walter.Social Cognitive Neuroscience of Empathy: Concepts, Circuits, and Genes,Emotion Reviews, January 24, 2012, doi:10.1177/1754073911421379
【2】Genetic and Environmental Influences on Marital Relationships.
【3】Predicting Success or Failure of Marital Relationships
【4】RICHARD E. MATTSON,LAURA E. FRAME,MATTHEW D. JOHNSON. Premarital affect as a predictor of postnuptial marital satisfaction, Personal Relationships, 24 November 2010,doi:10.1111/j.1475-6811.2010.01315.x
【5】rs1042778
【6】rs4686302
【7】Daniel B. Campbell, Dibyadeep Datta, Shaine T. Jones, et al. Association of oxytocin receptor (OXTR) gene variants with multiple phenotype domains of autism spectrum disorder, Journal of Neurodevelopmental Disorders, 2011 3:9071 doi:10.1007/s11689-010-9071-2
【8】René Hurlemann, Alexandra Patin, Oezguer A. Onur, et al. Oxytocin Enhances Amygdala-Dependent, Socially Reinforced Learning and Emotional Empathy in Humans, Journal of Neuroscience 7 April 2010, 30 (14) 4999-5007; doi:10.1523/JNEUROSCI.5538-09.2010
【9】Genetic moderation of sensitivity to positive and negative affect in marriage.
【10】How your genes could affect the quality of your marriage
Richard Mattson, February 8, 2019 6.31am EST
2019年3月2日 讯 /生物谷BIOON/ –酒精和烟草的使用与多种疾病发生有关,同时其也是诱发人群死亡的主要原因;近日,一项刊登在国际杂志Nature Genetics上的研究报告中,来自国外的研究人员通过收集120万人的数据进行分析,发现了与烟草和酒精使用量增加相关的多个基因,同时研究者还观察了这些基因与多种疾病风险发生相关的关联。
图片来源:CC0 Public Domain
研究者发现,人类基因组406个不同位点上的566个基因突变与人群烟草或酒精使用量有关,其中150个位点与烟草和酒精使用量存在直接关联。研究者根据标准酒精单位的数量来衡量人群的饮酒情况,同时以人群每天吸烟的数量来衡量烟草的使用量。研究者表示,有吸烟遗传倾向的研究组也在遗传上更倾向于患多种健康问题,比如肥胖、糖尿病及多种精神疾病等;而饮酒的遗传风险却与疾病风险降低直接相关,但这并不是说,摄入过多酒精就能够改善机体健康,研究者需要深入研究才能深入解析其中的复杂关联。
研究者在机体中发现烟草和酒精使用的多种天然信号制剂,包括与烟碱、多巴胺能和谷氨酸能神经传递有关的基因等,从某种程度上来讲,这或许能够帮助解释为何某些人更愿意寻找人工刺激。文章中,研究者发现,遗传风险和不同疾病发生之间的关联似乎在不同研究群体中变化不大。使某些人具有某种特点的遗传突变并不一定要表达或者具有生物活性,这依赖于多种因子,不同基因间的相互作用扮演着关键角色,而且社会状况也会影响人群酒精和烟草的使用情况,从而就会使得研究者更难得出准确的结论了。
本文研究中,研究人员对基因和环境因素的复杂性提出了新的见解,这些复杂性会迫使某些人比其他人更喜欢饮酒和吸烟,但其中某些与饮酒水平增加相关的基因却能够有效降低人群患某些疾病的风险。(生物谷Bioon.com)
原始出处:
Mengzhen Liu, Yu Jiang, Robbee Wedow, et al. Association studies of up to 1.2 million individuals yield new insights into the genetic etiology of tobacco and alcohol use, Nature Genetics (2019). DOI: 10.1038/s41588-018-0307-5

3月11日下午,墨子沙龙新春首场报告在上海图书馆举行,中国科学院神经科学研究所高级研究员、博士生导师仇子龙,同济大学特聘教授、博士生导师章小清,浙江大学生命科学研究院教授、研究员、博士生导师王立铭,在中国科学技术大学教授陈宇翱主持下,为600余名观众带来精彩的科普报告,围绕基因编辑、干细胞等大众关心的科学问题展开探讨,于细微之处探寻生命密码。同时,有近25万名观众通过网络直播实时聆听了本场报告。
“很多疾病由基因突变引起,能否修复基因突变成了治疗这些疾病的关键。”仇子龙介绍,修复基因本是一件及其困难的事情,但近年来科学家发明的叫做CRISPR/Cas的基因编辑工具令这件困难的事变得可行。它来源于细菌对抗噬菌体的防御系统,受其启发,人们开始于2012年发明基因编辑工具,并将其用于哺乳动物细胞定点基因的编辑。很快,这套工具不仅成为了基因科学家的必备武器,还有可能被用来修复基因突变、治疗遗传病。
仇子龙以杜氏肌营养不良症(DMD)和脊髓性肌肉萎缩症(SMA)的研究和治疗为例,展示了基因治疗针对遗传疾病发挥的惊人作用。
仇子龙团队毕业的博士与中科大薛天教授合作,通过对基因突变的准确修复,修正了小鼠视网膜细胞基因突变,使小鼠的眼睛重获光明,为相关疾病的治疗带来曙光。仇子龙表示,目前,很多过去认为的绝症,相关临床实验正在进行,最近三到五年之内,大批的基因治疗的药物即将上市,有望帮助到世界各地包括中国的病人。
章小清在报告中介绍,干细胞与万千物种的生长、发育、繁衍、衰老息息相关,有些生物甚至用干细胞进行组织的再生。对人类来说,是否可以利用干细胞技术来进行生命的重现、衰老的延缓、或者组织、器官的替代治疗呢?带着这些问题,章小清带来了一场有关干细胞研究的起源、发展、应用和思考的报告。
干细胞的发现起源于小鼠的畸胎瘤,科学家因此开始对干细胞进行研究。1981年,小鼠胚胎干细胞建成,17年后,人的胚胎干细胞才得以建立。此后,人们开始探索建立我们自身的干细胞,体细胞核移植技术、诱导多能干细胞、成体干细胞相继实现,都为干细胞的应用打下了基础。
章小清表示,在针对肿瘤干细胞的靶向治疗、细胞本质的探索、疾病的模拟、转基因动物的构建、细胞组织的再生等方面,干细胞研究都显示了不可替代的生命力。
王立铭的报告从去年11月世界上首例基因编辑婴儿引起轩然大波开始,指出人类对于遗传现象的探索从来都交织着光明与黑暗,科学和伦理因此紧密相连。
对于人类来说,基因决定人类形状。基因缺陷会导致人类各种遗传疾病。传统的基因治疗有一定局限,只能修补缺陷基因,但是对于一些由于基因上某些特定位点发生问题引发的病变束手无策。而得益于基因编辑的长足进步,人们开始可以对错误碱基进行剪切和编辑。
目前,科学界普遍认为,基因编辑应当被允许进入人类社会,用以消除镰刀形贫血病等毁灭性疾病。但是,基因编辑的未来必然引发社会的广泛讨论。从农业生产、疾病的预防和治疗的角度来说基因编辑必定会为人类带来福利,但是也不可避免为人类带来健康和社会格局上的风险,值得科学家和公众共同思考。
当天,3位科学家在圆桌论坛环节中就公众关心的基因编辑和干细胞研究的伦理及应用问题展开探讨。仇子龙认为,基因数据安全是至关重要的,建议个人妥善保管个人基因数据,也呼吁建立相关法律,保障基因数据安全。王立铭回答了听众的问题:治疗方法的选择一定要综合考量收益和风险。
据介绍,墨子沙龙于2016年,由中国科学院院士潘建伟发起,由中国科学技术大学主办,以中科大上海研究院为基地的公益科普论坛,旨在通过科普讲坛、和科学家面对面的方式,进行专业的科学启蒙。(生物谷Bioon.com)

近日,中国科学院昆明植物研究所副研究员张体操联合西藏大学、云南大学及国外多个实验室,对青藏高原特有分布的须弥芥进行了基因组适应性进化研究,为青藏高原植物适应极端环境的分子机制提供了新的线索。相关研究结果在线发表于《美国科学院院刊》。
据了解,须弥芥原本归在拟南芥属,1999年Ihsan Al-Shehbaz教授将其从拟南芥属中独立出来。中科院院士吴征镒认为须弥芥是拟南芥属在青藏高原特殊环境下能够适应高海拔极端环境的特化类群。因此,作为拟南芥的近缘物种,须弥芥有望成为极端环境适应性进化的新模式植物。在之前的研究中,团队利用转录组数据发现须弥芥的基因受到明显的自然选择作用。
张体操团队利用二代和三代高通量测序技术,组装得到了234.72Mb的须弥芥基因组,包括27019个预测的基因。同时他们利用4586个直系同源基因进行系统发育分析,发现须弥芥与荠菜最近缘,分化时间大约为8.8—12.2个百万年,而与拟南芥属分化时间约为12.7-17.2个百万年。
研究发现,青藏高原在上新世晚期至更新世快速隆升之后,须弥芥的LTR反转录转座子发生了明显的扩张,这可能与隆升后的环境适应有关。通过与近缘物种相比较,须弥芥基因组中抗病相关的基因家族发生了明显缩减,可能与青藏高原病原菌较少有关。同时,须弥芥中扩张的基因家族和受到强烈自然选择的基因都与泛素介导的蛋白水解和DNA损伤修复有关。这两个途径都是属于综合的抗逆过程,对于青藏高原复杂多变的特殊环境可能起到重要作用。
张体操说:“须弥芥与自交亲和性相关的雄蕊识别SCR基因变成了假基因,雌蕊识别SRK基因完全丢失,这是导致须弥芥自交亲和的根本原因,也有可能是适应青藏高原传粉昆虫少的一种策略。”
研究还发现在青藏高原的适应机制上,植物与动物在DNA修复途径、抗病途径方面有相似点,但它们在植物自交亲和性、植物激素途径方面存在不同。(生物谷Bioon.com)