2016年11月17日/生物谷BIOON/–在一项新的研究中,来自美国沙克研究所的研究人员发现基因编辑的圣杯—首次能够在基因组的靶位点上将DNA插入到非分裂细胞(non-dividing cell)中,其中非分裂细胞占成年器官和组织中的大多数。他们证实这种技术能够部分恢复失明的啮齿类动物的视觉反应。它将为基础研究和多种治疗视网膜疾病、心脏疾病和神经疾病等疾病的方法打开新的途径。相关研究结果于2016年11月16日在线发表在Nature期刊上,论文标题为“In vivo genome editing via CRISPR/Cas9 mediated homology-independent targeted integration”。
论文通信作者、沙克研究所基因表达实验室教授Juan Carlos Izpisua Belmonte说,“我们对我们发现的这项技术感到非常激动人心,这是因为它是我们之前不能够做到的。我们首次能够以未发生分裂的细胞为靶标,随心所欲地修饰它们的DNA。这项发现的可能应用是非常巨大的。”
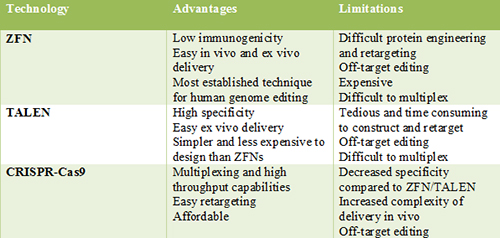
在此之前,修饰DNA的技术—如CRISPR-Cas9系统—已最为有效地利用分裂细胞(dividing cell)的正常复制机制在这些细胞(如在皮肤或肠道中的那些细胞)当中在发挥作用。沙克研究所开发的这种新技术在将新的DNA整合到体外培养的分裂细胞中的效率比其他方法高10倍,使得它成为一种大有希望的用于研究和药物开发的工具。但是,更为重要的是,这种新技术首次代表着科学家们成功地将一种新的基因插入到不再发生分裂的成体细胞(如在眼睛、大脑、胰腺或心脏中的那些细胞)中准确的DNA位点上,从而为在这些细胞中进行治疗应用提供新的可能。
为了做到这一点,研究人员瞄准一种被称作非同源末端连接(non-homologous end-joining, NHEJ)的DNA修复细胞通路,其中NHEJ通过将发生常规断裂的DNA链末端重新连接在一起对断裂的DNA进行修复。他们将这个过程与现存的基因编辑技术组合使用,从而成功地将新的DNA插入到非分裂细胞中的精确位点上。
论文共同第一作者、Izpisua Belmonte实验室资深研究员Keiichiro Suzuki说,“就对活的成年有机体的基因组进行基因编辑而言,利用这种NHEJ通路插入全新的DNA是革命性的。在此之前,没有人做到这一点。”
首次,研究人员对NHEJ通路进行优化,以便与CRISPR-Cas9进行组合使用,从而允许将DNA导入到基因组中非常准确的位点上。研究人员构建出一种定制的由一种核酸混合物组成的被称作同源非依赖性靶向整合(homology-independent targeted integration, HITI)的插入工具。他们随后利用一种惰性病毒将HITI携带的遗传指令运送到由人胚胎干细胞产生的神经元中。
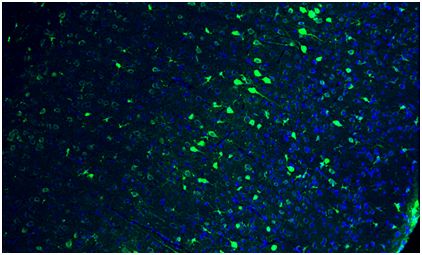
论文共同第一作者Jun Wu说,“这是首次表明HITI可能在非分裂细胞中发挥作用。”基于获得的这种成就,研究人员随后成功地将这种遗传指令运送到成年小鼠的大脑中。最终,为了探究将HITI用于基因替换疗法中的可能性,他们在患有视网膜色素变性—一种遗传性的视网膜退化疾病,可导致人失明—的模式大鼠体内测试了这种技术。在这次,研究人员利用HITI将一种功能性的Mertk基因拷贝运送到3周大的大鼠的眼睛中,其中Mertk是在视网膜色素变性中受到损伤的一种基因。当这些大鼠在8周大时,对它们的分析结果表明它们能够对光线作出反应,而且几项测试的结果表明它们的视网膜细胞发生愈合。
论文共同第一作者Reyna Hernandez-Benitez说,“我们能够改善这些失明大鼠的视力。这种早期的成功提示着这种技术是非常有希望的。”
研究人员的下一步将是改善HITI构建体的运送效率。正如所有的基因组编辑技术一样,获得足够的细胞来整入新的DNA是一大挑战。HITI技术的美妙之处在于它可适应于任何靶向基因组编辑系统,而不仅仅是CRISPR-Cas9。因此,随着这些系统的安全性和有效性得到改善,HITI的有效性也将会得到改善。
Izpisua Belmonte说,“如今,我们有一种技术允许我们修饰非分裂细胞中的DNA,修复大脑、心脏和肝脏中发生断裂的基因。它允许我们首次能够想象一下治愈我们之前不能够治愈的疾病,这是激动人心的。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎转载!点击 获取授权 。更多资讯请下载生物谷APP。
In vivo genome editing via CRISPR/Cas9 mediated homology-independent targeted integration
Keiichiro Suzuki, Yuji Tsunekawa, Reyna Hernandez-Benitez, Jun Wu, Jie Zhu, Euiseok J. Kim, Fumiyuki Hatanaka, Mako Yamamoto, Toshikazu Araoka, Zhe Li, Masakazu Kurita, Tomoaki Hishida, Mo Li, Emi Aizawa, Shicheng Guo, Song Chen, April Goebl, Rupa Devi Soligalla, Jing Qu, Tingshuai Jiang, Xin Fu, Maryam Jafari, Concepcion Rodriguez Esteban, W. Travis Berggren, Jeronimo Lajara, Estrella Nuñez-Delicado, Pedro Guillen, Josep M. Campistol, Fumio Matsuzaki, Guang-Hui Liu, Pierre Magistretti, Kun Zhang, Edward M. Callaway, Kang Zhang & Juan Carlos Izpisua Belmonte
 基因君官网
基因君官网