
上线新型国产测序仪,华大基因再攻上游垄断



有些人很容易适应轮班工作,但并不是每个人都可以处理不断打乱他们的日常节奏。 芬兰研究人员已经发现,褪黑激素受体基因影响对轮班工作的耐受性。
发表在《睡眠》杂志上的这项新的研究是第一次系统地研究造成对轮班工作耐受性较差的基因因素。 覆盖了整个基因组的研究发现,褪黑激素受体1A(MTNR1A)的常见变异基因与轮班工作者工作疲惫相关联。
轮班工作经常扰乱了昼夜节律,从而导致睡眠障碍和日间疲劳。
该研究由芬兰赫尔辛基大学教授Tiina Paunio领导,涉及很多从事不同轮班工作的工人。由工人报告的工作疲惫的差异性与整个基因组的遗传差异形成强烈对比。
与褪黑激素受体基因的相关性在2000年国民健康调查中的一组包括176名轮班工人中被发现。 这一相关性还在2000年健康调查的其他577名轮班工人以及从事护理和航空的轮班工作者中被发现。
该研究还确立了褪黑激素受体1(MTNR1A)基因的风险变异可能与调控MTNR1A基因序列的DNA甲基化以及MTNR1A基因的弱表达有关系。 DNA的甲基化是调节基因组功能的一种表观遗传机制,不仅受DNA序列变化的影响, 而且还受环境因素如昼夜节律波动的影响。
由于导致较少的褪黑激素受体产生,风险基因的变异可能导致自然褪黑激素信号(稳定昼夜节律的调节机制之一)较弱。
MTNR1A基因变异的影响可以解释夜间暴露于灯光中对轮班工作者昼夜节律破坏的程度。 “变异的发现只能解释一小部分个体之间的差异,它不能作为确定一个人对轮班工作忍受程度的基础,”Paunio指出。(生物谷Bioon.com)

2016年11月6日/生物谷BIOON/–我们通常认为突变是我们的基因发生的错误,这种错误会让我们患病。但是并不是所有错误都是不好的,一些错误甚至能够抵消或抑制那些已知导致疾病的突变的负面影响。人们对这个被称作遗传阻遏(genetic suppression)的过程了解甚少,但是当来自加拿大多伦多大学的研究开始揭示它背后的一般规则时,这种情况将会改变。
来自多伦多大学唐纳利中心和分子遗传学系的Brenda Andrews教授、Charles Boone教授和Frederick Roth教授与来自美国明尼苏达大学双城校区的Chad Myers教授合作开展研究,汇集了细胞中首个完整的抑制性突变组合。他们的发现可能有助解释抑制性突变与导致疾病的突变相结合如何减轻疾病的打击,或者甚至完全抵抗它。相关研究结果发表在2016年11月4日那期Science期刊上,论文标题为“Exploring genetic suppression interactions on a global scale”。
这是生物学中令人好奇的部分,仅当更多健康的人的基因组被测序后才能真相大白。在他们当中的一些非常幸运的人尽管携带导致囊性纤维化和范可尼贫血等虚弱性疾病的灾难性突变,但是仍然能够躲过这一劫难,保持健康,并且表现出疾病恢复性。怎么可能是这样的呢?
Roth说,“我们真地不能理解为何一些携带破坏性突变的人患病,而另一些人却不会患病。一些原因可能是来自环境的,但是许多原因可能是存在抑制首个突变的影响的其他突变。”
想象一下呆在一间自动调温器坏了的房间,它非常热。为了凉爽,你能够将自动调温器修复好,或者你能够仅仅打开一扇窗户。这就是遗传阻遏让携带破坏性突变的细胞保持健康的工作方式。它为理解和甚至可能治疗遗传病开启一种新的方式。
Boone实验室博士后研究员Jolanda van Leeuwen博士说,“如果我们知道发生这些抑制性突变的基因,那么我们能够理解它们如何与这些致病性基因存在关联,以及可能指导未来的药物开发。”
但是发现这些突变也不是易事。在人体中,它好比是大海捞针。理论上,一种抑制性突变可能是人DNA的几十万种碱基拼写错误中的任何一种,并且是散落在2万种人基因之中,这就使得每个人的基因组都比较独特。对它们进行测试将是不现实的。
Van Leeuwen说,“诸如此类的研究从没有在全局水平上开展过。鉴于在人体内开展这些实验是不可能的,我们使用酵母作为一种模式生物,在酵母中,我们能够精确地知道突变如何影响细胞的健康。”仅有6000种基因的酵母细胞相对于人细胞而言更加简单,但是相同的基本遗传规则都是通用的。再者,为了研究一种突变的最为严重的形式—基因功能完全缺失,从酵母细胞中移除任何一种基因是相对容易的。
为此,研究人员采取一种双管齐下的方法。一方面,他们分析了所有发表的针对已知的酵母基因之间存在的抑制关系的数据。尽管这会提供有价值的信息,但是这些结果不可避免地偏向最为流行的基因—科学家们已详细研究过的基因。为此,Van Leeuwen和同事们也通过测量当酵母细胞本身携带一种破坏性突变或者还携带另一种突变时这些细胞如何好地生长,进行无偏差地分析。鉴于有害突变会延缓酵母细胞生长,它们生长率的任何改进是由于第二个基因上的抑制性突变导致的。这些实验揭示出这些破坏性突变存在上百种抑制性突变。
重要的是,无论采用哪种方法,这些数据指向相同的结论。为了发现抑制基因,研究人员经常不需要远离携带破坏性突变的基因。这些基因往往在细胞中具有类似的作用—这要么是由于它们的蛋白产物在物理上位于相同的位置,要么是由于它们在相同的分子通路中发挥作用。
Boone说,“我们发现遗传阻遏的基本原则,并且证实破坏性突变和它们的抑制性突变通常是在存在功能性相关的基因中发现的。当寻找人体内遗传疾病的抑制基因时,我们如今不是大海捞针,而是能够缩小我们的搜寻范围。我们从一个涵盖2万种基因的搜索区域缩小到一个涵盖几百种或者甚至几十种基因的搜索区域。这是一个很大的进步。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎转载!点击 获取授权 。更多资讯请下载生物谷APP。
Exploring genetic suppression interactions on a global scale
Jolanda van Leeuwen, Carles Pons2,3,*, Joseph C. Mellor1,4,†, Takafumi N. Yamaguchi1,4,5, Helena Friesen1, John Koschwanez6, Mojca Mattiazzi Ušaj1, Maria Pechlaner7, Mehmet Takar8, Matej Ušaj1, Benjamin VanderSluis2,‡, Kerry Andrusiak1,5, Pritpal Bansal1,4, Anastasia Baryshnikova9, Claire E. Boone1, Jessica Cao1, Atina Cote1,4, Marinella Gebbia1,4, Gene Horecka1, Ira Horecka1, Elena Kuzmin1,5, Nicole Legro1, Wendy Liang1, Natascha van Lieshout1,4,5, Margaret McNee1, Bryan-Joseph San Luis1, Fatemeh Shaeri1,4, Ermira Shuteriqi1, Song Sun1, Lu Yang1, Ji-Young Youn4, Michael Yuen1, Michael Costanzo1, Anne-Claude Gingras4,5, Patrick Aloy3,10, Chris Oostenbrink7, Andrew Murray6, Todd R. Graham8, Chad L. Myers2,11,§, Brenda J. Andrews1,5,§, Frederick P. Roth1,4,5,11,12,§, Charles Boone

研究人员表示,基因疗法有望可以治愈一种遗传性皮肤病,这种皮肤病可以导致水疱。
早期的临床试验中,斯坦福大学医学院的研究人员在4名隐性营养不良性大疱性表皮松解症患者身上测试了这种疗法。
研究人员表示,患有隐性营养不良性大疱性表皮松解症的人无法合成将上下层皮肤连接到一起的蛋白。即使碰到很小的摩擦力,这些皮层就会滑动而产生水疱。最糟糕的情况是,患者在婴儿期就死亡了。
本研究中,将患者自身遗传性正确的皮肤移植到皮肤病导致的伤口上。移植的皮肤可以促进伤口愈合,而且耐受性良好。
皮肤科副教授Jean Tang博士称,我们的I期临床试验显示,这种疗法很安全,我们很幸运地看到一些很好的临床结果。有些病例中,已经5年没有愈合的伤口成功地被基因疗法治愈了。这对于患者来说,意味着生活质量的大幅提高。
下一步就要评估这个疗法对13岁以上的患者的效果。可以治疗儿童,就可以预防严重慢性伤口和伤疤的形成。
但是,还需要更多的试验,这个疗法才能成为广泛接受的临床常规疗法。
研究已经发表在11月1日的《美国医学协会》上。(生物谷Bioon.com)

图片来源:medicalxpress.com
2016年11月4日 讯 /生物谷BIOON/ –近日,刊登在国际杂志Nature上的一项研究报告中,来自西南医学中心等机构的研究人员通过研究鉴别出了两个关键的核心基因,这两个基因能够帮助调节机体深度睡眠和做梦的水平,相关研究或为阐明相关的基因控制睡眠的网络提供新的线索。此前研究者通过对小鼠进行研究发现了能够控制机体快速眼动睡眠的基因,同时该基因还能够诱导深度睡眠,而第二个基因能够控制机体对快速眼动睡眠的需求量,相关研究为科学家们提供了一个关键的切入点来帮助解释睡眠工作的机制,同时研究者还鉴别出了治疗睡眠障碍的潜在靶点。
研究者Joseph S. Takahashi表示,这项研究仅仅是个开始,我们认为,这两个基因是调节机体睡眠众多基因中两个,此前我们通过研究鉴别出了调节机体觉醒和睡眠之间切换开关的基因,但目前我们并不清楚控制快速眼动睡眠需求和驱动的机制。随后研究人员利用了一种遗传学方法对8000只小鼠进行了睡眠障碍的筛查,并且利用脑电流描记术来监测小鼠的脑电波。
正常的睡眠模式包括被睡眠期长的非快速眼动睡眠所包围的短期快速眼动睡眠,同时这种模式还能够解释大部分年轻人大约四分之一的夜晚睡眠的状况;很多模式的睡眠障碍都会扭曲这种正常的模式,如今由于Sik3和Nalcn这两个基因被鉴别,因此并没有证据将这两个基因同人类已知的睡眠障碍相连接。然而关于快速眼动睡眠的重要性和角色目前还一直存在争议,很多科学家们都认为休息的阶段主要参与了机体情绪记忆的形成以及处理负面的经历,然而缺乏快速眼动睡眠或许就会导致诸如创伤后应激障碍(PTSD)的发生。
Yanagisawa说道,从理论上来讲,本文研究或可帮助开发新型的睡眠调节性药物,由Sik3和Nalcn基因产生蛋白或许就会成为未来新型疗法开发的分子靶点。20年前我们利用遗传学方法发现Clock基因能够调节机体的生物钟,随后我们的研究团队还发现了超过20个其它相关的基因。我们希望这种对睡眠基因的筛选能够帮助发现更多未知的奥秘。
目前研究者并不清楚如此庞大的基因网络如何调控着机体的睡眠,而且他们仅发现了一部分时钟基因在大型的基因网络中扮演着至关重要的角色;Takahashi说道,很多年来他们一直想进行一项研究,对睡眠突变体进行遗传筛选,但目前他们必须克服一些逻辑上的问题,并且进行更大的努力;很多在小鼠中进行的研究都并没有使用超过几十只动物进行研究,但研究者Takahashi就能够不断扩大并且优化实验室的能力来对大量的小鼠进行筛选。
对8000只小鼠进行筛选研究在很多人看来是一项非常庞大的工作,但研究者解释道,我们必须对每只小鼠进行操作来进行脑电图的读数以及后续的分析,这从技术上来讲是极具挑战性的。(基因宝jiyinbao.com)
本文系生物谷原创编译整理,欢迎转发,转载需授权!点击 获取授权 。更多资讯请下载 生物谷APP.
Forward-genetics analysis of sleep in randomly mutagenized mice
Hiromasa Funato, Chika Miyoshi, Tomoyuki Fujiyama, Takeshi Kanda, Makito Sato, Zhiqiang Wang, Jing Ma, Shin Nakane, Jun Tomita, Aya Ikkyu, Miyo Kakizaki, Noriko Hotta-Hirashima, Satomi Kanno, Haruna Komiya, Fuyuki Asano, Takato Honda, Staci J. Kim, Kanako Harano, Hiroki Muramoto, Toshiya Yonezawa, Seiya Mizuno, Shinichi Miyazaki, Linzi Connor, Vivek Kumar, Ikuo Miura et al.

近日,证券时报消息称,“证监会统计资料显示,截至10月27日,深圳华大基因IPO审核状态显示为中止审查。中止情形显示为:申请文件不齐备等导致审核程序无法继续。”华大基因为国内基因测序龙头,公司于去年12月递交公开招股说明书(申报稿),医谷也曾报道过,见《华大基因终于要上市了,证监会发布预披露招股书》。
今日(11月3日),华大基因公司发布公告,回应了此事。公告说明如下:
近日,有媒体报道,本公司因IPO文件不齐遭中止审查。公司在获悉上述报道内容后,经核实,说明如下:
公司IPO中介机构原经办人员因职业发展等个人原因,无法再作为经办人员为公司提供服务,根据相关法规要求,更换中介机构经办人员需要履行中止审查程序,因而公司IPO中止审查,并非IPO文件不齐。
近日,经办人员已更换完毕,公司已收到恢复审查通知,预计近期会公告更新后的审核状况。
公司IPO正在稳步进行中。公司将根据进展情况,依据证监会有关法律法规及相关规定严格履行相应的决策、审批程序,并及时履行信息披露义务,公司所有信息均以公司公告为准。
特此公告。
深圳华大基因股份有限公司
二〇一六年十一月三日

公开资料显示,被誉为“国内基因测序龙头”、“基因测序界的腾讯”的华大基因于2015年12月以2456万的年利润入IPO创业板排队序列。
另据悉,中国证监会《发行监管问答—关于首次公开发行股票中止审查的情形》新股发行企业具有四类情形之一将中止审查
在审核过程中,有些企业因为出现了一些客观情况,使得审核程序无法继续,或者存在对其信息披露的真实性、准确性、完整性的质疑且有一定的线索,需要通过必要的核查来查清事实。在这些情况下,为维护正常的审核秩序,本着对发行人和投资者负责的态度,证监会将这些企业列入中止审查的名单。主要包括四类情形:
第一,申请文件不齐备等导致审核程序无法继续的情形。具体情况包括:1、对有关法律、行政法规、规章的规定,需要请求有关机关作出解释,进一步明确具体含义。2、发行人申请文件中记载的财务资料已过有效期。3、发行人及其中介机构未在规定的期限内提交反馈意见回复。4、发行人发行其他证券品种需要履行信息披露义务,导致审核程序冲突。5、负责本次发行的保荐代表人发生变更,会计师事务所、律师事务所或者签字会计师、律师发生变更,需要履行相关程序。
第二,发行人主体资格存疑或中介机构执业行为受限导致审核程序无法继续的情形。具体情况包括:1、发行人、发行人的控股股东、实际控制人及发行人的保荐机构或律师因涉嫌违法违规被行政机关调查,或者被司法机关侦查,尚未结案。2、保荐机构或其他中介机构被中国证监会依法采取限制业务活动、责令停业整顿、指定其他机构托管、接管等监管措施,尚未解除。
第三,对发行人披露的信息存在重大质疑需要进一步核查的情形。1、发行人申请文件中记载的信息存在自相矛盾、或就同一事实前后存在不同表述且有实质性差异。2、根据发行申请文件披露的信息,对发行人是否符合发行条件明显存疑,需要进一步核实。3、媒体报道、信访举报反映或者通过其他途径发现发行人申请文件涉嫌违法违规,或者存在其他影响首次公开发行的重大事项,经初步核查无法澄清。
第四,发行人主动要求中止审查或者其他导致审核工作无法正常开展的情形。
发行人首次公开发行股票申请中止审查后,如何才能恢复审查?包括以下情况:
发生中止审查事项后,发行人及中介机构需及时补充相关材料或提供书面说明,证监会将视情况依照有关规定分别采取要求发行人和中介机构自查、委托其他中介机构或派出机构核查、或者直接现场核查等措施。发现存在违规行为的,将对相关责任人采取相应监管措施;发现违法犯罪线索的,将移送稽查部门调查或移送司法机关侦查。
中止审查后,如果中止审查事项已经消除、发行人及中介机构已经进行澄清或者采取纠正措施的,恢复审查。
发行人申请文件中记载的财务资料已过有效期且逾期3个月未更新的,直接终止审查。
中止审查期间,发现发行人不符合《证券法》、《首次公开发行股票并上市管理办法》及《首次公开发行股票并在创业板上市管理暂行办法》规定的发行条件的,将依程序终止审查或者做出不予核准的决定。
申请人主动要求中止审查的,申请恢复审查时,应当提交书面申请,经审核同意后恢复审查。
恢复审查后,将参照发行人首次公开发行申请的受理时间安排其审核顺序。
显然,华大基因是因为第一种情况导致“IPO中止”,虽然引起了不少业界关注,但是作为国内测序龙头企业的华大基因没有受到影响,IPO将继续正常进行。(生物谷Bioon.com)


在墨西哥湾发现的双头公牛鲨幼体

出生时长有两个头的动物十分罕见
据国外媒体报道,早在多年以前,科学家就记录了一些双头动物的罕见例子。比如,20世纪40年代,凯布尔(L E Cable)就描写了一条长着两个头的海龙胚胎。他将其称为“小怪物”。更近的例子是,伦敦帝国学院的发育生物学家阿布赞诺夫(Arkhat Abzhanov)在实验室中观察到了许多双头动物。借助现代遗传学的知识,他对导致这一现象的基因突变和细胞置换过程进行了观察。类似的例子或许曾为古代传说的写作者提供了灵感。
事实上,双头甚至三头动物不是就会在自然界或人工圈养环境中出现。有趣的是,这种现象似乎并不局限于某一类动物。就以鱼类说起。2013年,有人在墨西哥湾发现了一只双头公牛鲨幼体。
2014年,人们在土耳其的一个沙滩上发现了海洋哺乳动物的例子——一只双头海豚。这两个例子似乎都是连体双胞胎,即从同一个受精卵发育而来,但没有在受精之后完全分开。人类中也有这样的例子。通常情况下,连体后代不只是长有两个头,而是具有双份的特定内脏器官,甚至是肢体。
一组著名的实验显示,限制受精卵部分分裂——导致产生连体双胞胎的原因——是可能的。20世纪初期,一位名叫汉斯·斯佩曼(Hans Spemann)的生物学家进行了这组实验。他对胚胎发育的过程十分感兴趣。他用一束人的体毛将非常初期的蝾螈胚胎绑在一起,结果发现蝾螈会因此长出两个头——两个为了同一个身体争夺食物的头。他将此称为“同个地方的两个自私者”。

双头生物并不仅仅是传说

连体双胞胎是从同一个受精卵发育而来的
事实上,双头动物的名单相当长,包括龟类、蛇类甚至还有猫。我们还知道,这一现象并不是今天才有。古生物学家已经发现了数百万年前的双头胚胎化石,有多种机制都可以导致出现不止一个头或一张脸。广义上来说,动物体的头部是趋同演化的例证,即完全不同的动物类群中会独立演化出相同的特征。无脊椎动物和脊椎动物都从拥有头部的特征中获益,但它们具有不同的祖先世系。头部是非常有用的适应特征,非常多动物种类都具有头部。
“拥有(头部)实际上是很有用处的,”阿布赞诺夫解释道,“你进入新环境是总是先把头伸进去。”这也是为什么众多感觉器官——眼睛、耳朵、鼻子和嘴巴等——都分布在头上的原因。
脸的形状和组成正确与否取决于动物体的基因,其中一种基因的作用尤其重要,特别是对脸部宽度的影响。该基因被奇怪地称为“Sonic Hedgehog”(刺猬索尼克),或者简称为SHH。这一名字来源于一组“刺猬”(hedgehog,HH)基因,首先是在果蝇中得到描述的。HH基因的突变导致果蝇出生时具有棘刺状的结构,看起来很像小刺猬。
拥有SHH基因的是脊椎动物,如果胚胎发育过程中,由SHH基因介导的hedgehog信号通路变弱,那动物的头部就会变得越来越窄。有些情况下甚至会开始塌陷,使动物出生时只有一只眼睛,就像长着一个独眼巨人的头。事实上,一种被称为环巴胺(cyclopamine)的物质就会导致牲畜(比如绵羊)出现这种畸形。印第安鹿食草中就含有这种物质,怀孕的雌性动物有时会将其吃到体内。
如果增强SHH信号会如何呢?这会导致相反的结果——头部会变宽直到出现两个脸部,这种变异很罕见,但是在家养动物和野生动物中都有报道。
当然,从技术上来说,这一过程只会导致“双面”动物的出现,而不是出现双头动物。阿布赞诺夫发现在动物发育早期的另一个奇妙变化,对于从一个身体上长出另一个完全独立的颈部和头部至关重要。

这只双头蝾螈并没有存活太久

传说中九头蛇的血液具有极强的毒性
头部与身体的其他任何结构一样,都需要被触发(才能发育)。很早期的胚胎中有一群细胞,我们称之为组织者,事实上,正是斯佩曼的蝾螈胚胎研究最终揭示了这些细胞的行为方式。如果你将这群细胞取出来,移植到一只青蛙的胚胎中,那它就会长出两个头。也就是说,这群细胞释放出了一种信号,告诉动物体再长出一个头来,连体双胞胎的出现也是由于这一过程,有时候,通过注入或切开另一个胚胎的方法,可以将这群关键的细胞移植到另一个胚胎之中。这就像一场生物学上的偷渡。
研究者越来越接近这些异常现象在发育过程中出现的原因,温度似乎是一个重要的因素。他和同事们常常从养鸡场得到受精卵,之后这些受精卵发育而成的胚胎会在实验室中接受观察。在炎热时期,他的团队注意到了一些奇怪的事情。
如果温度在30摄氏度以上,我们那星期收到的那窝蛋就会出现更高的畸形率——包括双头现象,有趣的是,这一情况在其他地方也发生过。一位生物学家发现, 较高的水温会引起双头斑马鱼的发育。这些事情发生的原因是什么,目前还没有定论,但更多关于温度对畸形影响的研究正在进行中。
生物学或许启发过传说,但反过来说也对,传说也启发过生物学。1758年,九头蛇的一些形象启发了瑞典植物学家兼动物学家卡尔·林奈(Carl Linnaeus),帮助他为一类微小的水生动物——水螅——命名。这些小生命非常有意思,因为它们具有许多像蛇一样的附肢,还具有再生的能力——就像九头蛇面对赫拉克勒斯时那样。
不过,有一件事情要注意:许多双头动物,如连体双胞胎,并不具有很高的存活率。它们能活过胚胎期已经非常罕见了,活到成年的更少之又少。2014年的一个例子展示了生物体生长时的持续发育会给多头生物带来多么巨大的压力。以色列海法大学的一个实验室报道了一只双头蝾螈,它获得了大量的媒体关注,但并没能存活太久。
双头蝾螈的例子并不常见,它在幼体时还挺好的,但变态期之后它就死了。蝾螈在变态成为成体之前,一直是保持蝌蚪的形态,变态时才失去鳃和鳍。它们的头部也会经历许多变化。眼睛的发育、舌头和牙齿的出现,以及嘴巴变得更宽。或许是这些变化导致了这只双头蝾螈的死亡,答案尚不得而知。
这些多头怪物的传说显示出人类对多头动物的不安和恐惧。对于多头动物,还有许多等待解决的问题,但考虑到极低的存活率——无论是圈养还是野生条件——现实生活中想找到它们的机会微乎其微。
我们只能猜测那些经典传说的作者是如何获得灵感的。情况有可能是,古时候有人无意间在野外碰见了一只双头动物,然后添油加醋,很夸张地讲述了这些动物的故事。最终,这些故事演变成了广为流传的神话传说,直到今天还激发着人们的想象力。
相关会议推荐

2017生物样本库综合应用与发展论坛
会议时间:2017.1.06-2017.1.07 会议地点:上海

图片来源:www.sciencedaily.com
2016年11月1日 讯 /生物谷BIOON/ –近日,来自布莱根妇女医院的研究人员通过研究发现了两个治疗动脉疾病(比如动脉粥样硬化)的潜在药物靶点,通过利用蛋白质组学对大量分子进行筛选,研究者鉴别出了两种PARP家族蛋白:PARP9和PARP14,这两种蛋白或许能够作为巨噬细胞激活的调节子,而巨噬细胞的激活同动脉疾病的发生直接相关,相关研究刊登于国际杂志Nature Communications上。
虽然巨噬细胞的激活机制至今仍然没有被完全阐明,此前有研究表明,巨噬细胞在动脉粥样硬化和其血栓并发症发生过程中扮演着重要作用,本文中研究者Masanori Aikawa博士及其同事在蛋白质水平上对动脉粥样硬化进行了研究,来确定到底是哪种分子参与了巨噬细胞的调节。
最后研究者将目光锁定到了两种蛋白质上,他们沉默了巨噬细胞中每一种基因的表达,结果发现,抑制PARP14或许就能够增加巨噬细胞的表达,同时抑制PARP9就会产生相反的效应。研究者希望这种基于假设产生的方法能够简化药物开发的漫长过程;同时他们还利用了一种系统性的方法,而这取决于网络分析,这种分析就能够帮助预测哪种通路很有可能会控制所研究的效应以便研究者能够优先考虑这些途径。
下一步研究者Aikawa和其同事计划继续深入研究来开发治疗动脉粥样硬化及其相关疾病的靶向性疗法。Aikawa说道,巨噬细胞的激活不仅在动脉疾病发病过程中发挥着重要作用,而且对于研究多种炎性疾病及自身免疫疾病也至关重要;本文的研究结果或许能为我们提供重要的线索来阐明动脉粥样硬化相关疾病的发病机制,同时帮助开发更多的新型疗法。(基因宝jiyinbao.com)
本文系生物谷原创编译整理,欢迎转发,转载需授权!点击 获取授权 。更多资讯请下载 生物谷APP.
PARP9 and PARP14 cross-regulate macrophage activation via STAT1 ADP-ribosylation
Hiroshi Iwata, Claudia Goettsch, Amitabh Sharma, Piero Ricchiuto, Wilson Wen Bin Goh, Arda Halu, Iwao Yamada, Hideo Yoshida, Takuya Hara, Mei Wei, Noriyuki Inoue, Daiju Fukuda, Alexander Mojcher, Peter C. Mattson, Albert-László Barabási, Mark Boothby, Elena Aikawa, Sasha A. Singh & Masanori Aikawa
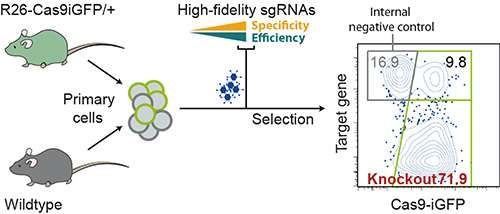
2016年11月1日/生物谷BIOON/–为了利用CRISPR-Cas9基因编辑系统切割基因,人们必需设计一种与靶基因的DNA相匹配的RNA序列。大多数基因具有上百个这样的在基因组中的活性和独特性上存在差异的序列。因此,寻找最佳的序列很难通过手工实现。一种新的“CrispRGold”程序有助科学家们鉴定出最为高效的和最为特异性的RNA序列。这种程序是由德国马克斯-德尔布吕克分子医学中心科学家Klaus Rajewsky教授领导的一个研究团队开发的。该团队也开发出一种新的已携带Cas9蛋白的模式小鼠。将这种模式小鼠和这些可靠的RNA序列结合在一起导致原代细胞中的基因高效地失活。这就使得研究人员能够发现参与免疫细胞调节的新基因。
对很多分子生物学家而言,发现这种CRISPR-Cas9基因编辑系统代表着研究上的一种新的里程碑:最终,基因组DNA能够被高效地和高精准地切割,从而能够让基因失活、修饰或重新导入。
这仅需一种将Cas9酶带到将被切割的DNA位点上的RNA片段。这种RNA片段被称作单向导RNA(sgRNA),含有长20个碱基(A、U、C或G)的与基因组靶位点互补的序列。在此之前,科学家们不得不通过手工费力地选择或者利用多种在线工具选择sgRNA。在某些情形下,人们并不确定所选的sgRNA是否将Cas9酶携带到基因组上合适的位点或者一种类似的但不是所想要的位点,以及这种sgRNA的效率是否比较高。
这种新的“CrispRGold”程序使得让特定基因失去功能变得更加简单。它寻找确定的DNA靶序列以便鉴定出进行切割的最佳位点并且提示一种在遗传物质上独特的仅运送Cas9蛋白到所需位点上的sgRNA序列然后能够切割靶基因以至于它不能够发挥功能。这种程序是基于实验数据和这些序列的独特性和其他性质而被开发出来的。
通过与Van Trung Chu博士合作,来自Rajewsky教授领导的这个团队的博士生Robin Graf在小鼠的B细胞中测试了这个系统。这些细胞不能够在体外培养非常长的时间,这是因为它们不会它们的自然环境外存活较长的时间。因此,基因在很多B细胞中必需尽可能快地失活以便研究它们的功能。Chu通过培养一种产生大量的但是具有良好数量耐受性的Cas9蛋白的转基因小鼠品系而实现这一点。
研究人员随后从这些小鼠体内分离出B细胞,将单个基因特异性的sgRNA运送到这些细胞中。Graf说,利用CrispRGold程序设计出的sgRNA在平均80%的这些细胞中高重复率地破坏这些靶基因。“在这种类型的低通量实验中,高效率和低错误率是绝对必要的。”
研究人员利用他们的新方法鉴定出许多种之前未知的参与B细胞发育的基因。Graf说,这种CrispRGold程序如今将被发布到网上,这样它能够被全世界的科学家们使用:“这种程序能够轻松地用于来自一系列有机体中的其他类型的细胞中。它也可能在临床应用中具有重要意义—它将序列独特性视为一种高度优先因素,因而使得对潜在不想要的基因的修饰最小化,这也是在基因疗法中必需不惜一切代价加以避免的。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎转载!点击 获取授权 。更多资讯请下载生物谷app。
Efficient CRISPR-mediated mutagenesis in primary immune cells using CrispRGold and a C57BL/6 Cas9 transgenic mouse line
Van Trung Chu, Robin Grafa,1,2, Tristan Wirtza, Timm Webera, Jeremy Favreta,b, Xun Lia, Kerstin Petscha, Ngoc Tung Trana, Michael H. Siewekea,b,c,d, Claudia Bereke, Ralf Kühna,f, and Klaus Rajewsky