科学家发现,晚睡晚起可能是由基因决定的。

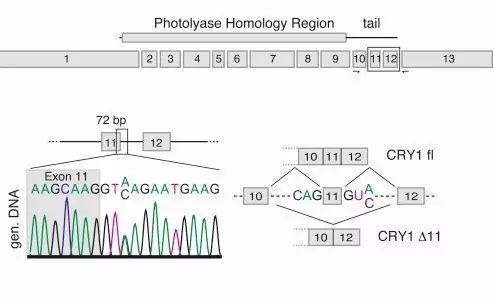
科学家发现,晚睡晚起可能是由基因决定的。


英格兰牛津2016年9月27日电 /美通社/ — 分子遗传学公司Oxford Gene Technology(牛津基因技术公司,简称OGT)已推出其SureSeq myPanel?新一代测序定制肿瘤探针组合库,为科学人员提供与他们研究相关的完全定制的预优化新一代测序探针组合库。这个完整的基因内容库覆盖主要的肿瘤类型,包括髓样白血病、慢性淋巴细胞白血病、卵巢癌和乳腺癌。通过利用基于杂交技术的捕获,这些组合库能够提供无与伦比的覆盖完整性和一致性,并且定期更新,最大程度上与当前的研究相结合。
(图标:http://photos.prnewswire.com/prnh/20160909/406091LOGO )
SureSeq myPanel新一代测序定制肿瘤探针组合库提供完整且一致的基因覆盖,包括高GC含量的基因。研究人员可以只针对他们感兴趣的区域选择探针,并且同样可以获得完整的数据。规模更小的高度定制、预优化组合库还可实现更高的吞吐量,且只需最短的验证时间。随着OGT与专家探讨之后不断添加新的探针,这些组合库可被替换或扩大,而所需费用与固定组合库相比却低的多,确保新一阶段的研究顺利进行。
一直开展骨髓增殖性肿瘤组合库试验的西密德兰地区遗传学实验室(West Midlands Regional Genetics Laboratory)研发科学人员Anna Skowronska表示:“我们对SureSeq组合库的表现非常满意。它与我们的其它技术完全一致,能够检测出所有已知基因突变,敏感度高达1%,包括检测出ddPCR由于引物二次突变而未检测出的JAK2 V617F突变。该组合库还在低水平的JAK2 V617F突变样本中检测出其它基因的突变,并论证了等位基因频率与ddPCR的定量分析之间良好的相关性。我们计划在不久的将来采用该组合库。”
OGT高级产品经理大卫-库克(David Cook)称:“凭借我们的SureSeq myPanel新一代测序定制肿瘤组合库,研究人员能够根据他们的具体要求轻松选择探针,并且可以在需要时对该组合库进行更新,添加新的内容。我们致力于研发的承诺意味着内容会定期更新,如果客户感兴趣的特定区域尚不可用,他们可提出相关开发要求,并将在约数周后获得内含预优化探针的完全定制组合库。”
详情请访问:http://www.ogt.com/sureseq。
SureSeq?仅用于研究,不用于临床诊断。
相关会议推荐

2016肿瘤代谢与营养研讨会
会议时间:2016.11.25-2016.11.26 会议地点:苏州
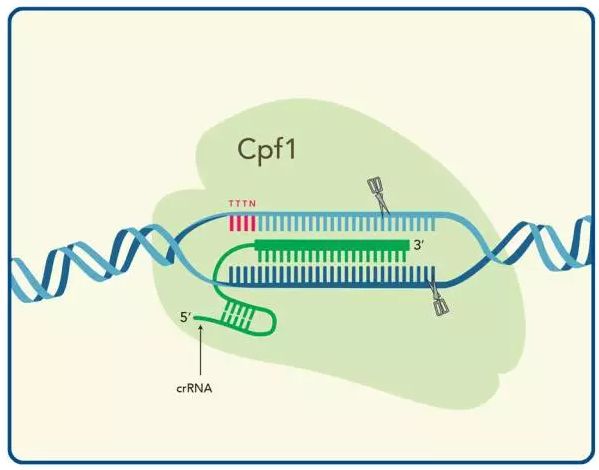

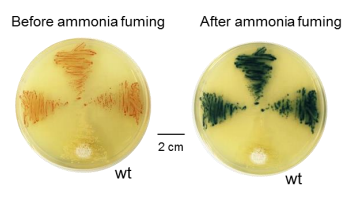
2017年4月13日/生物谷BIOON/—为了抵抗疾病,很多医药库中的武器是从细菌当中获得的。如今,利用CRISPR-Cas9基因编辑技术,研究人员揭示出沉默基因中隐藏着的更多潜在的宝藏。
作为一类常见的细菌,链霉菌被用来产生很多作为抗生素、抗癌试剂和其他药物的化合物。在一项新的研究中,来自美国伊利诺伊大学和新加坡科技研究局的研究人员利用CRISPR-Cas9技术激活链霉菌中不表达的或者说沉默的基因簇。相关研究结果于2017年4月10日在线发表在Nature Chemical Biology期刊上,论文标题为“CRISPR–Cas9 strategy for activation of silent Streptomyces biosynthetic gene clusters”。论文通信作者为伊利诺伊大学厄巴纳-香槟分校化学与与生化分子工程系教授Huimin Zhao。
Zhao说,“在过去,科学家们仅筛选细菌在实验室中产生的天然产物以便寻找新的药物。但是自从细菌基因组被测序以来,我们就意识到我们仅发现这种基因组编码的天然产物的一小部分。”
“绝大多数生物合成基因簇在实验室条件下并不表达,或者非常低水平地表达。这就是为什么我们称它们是沉默的。存在大量的新药物和新知识等待我们从这些沉默的基因簇中去发现。它们真地是隐藏的宝藏。”
为了挖掘未发现的基因组宝藏,这些研究人员首先利用计算工具鉴定出沉默的生物合成基因簇,即一小群参与制造化学产物的基因。他们随后利用CRISPR/Cas9技术将一种强启动子序列插入到他们想要激活的基因前面,促使细菌细胞制造这些基因簇编码的天然产物。
Zhao说,“对CRISPR/Cas9技术而言,这是一个较新的研究方向。大多数CRISPR/Cas9相关的研究着重关注生物医学应用,如治疗遗传病,但是我们将它用于药物开发。”他的实验室是首次将这种CRISPR系统用于链霉菌中。“在过去,启动或关闭链霉菌中的特定基因是比较困难的。如今,利用CRISPR/Cas9,我们能够高效地靶向几乎任何一个基因。”
这些研究人员成功地激活了一些沉默的生物合成基因簇。为了寻找候选药物,每个天然产物需要加以分离和研究以便确定它发挥什么功能。为此,从一种沉默的生物合成基因簇经激活产生的新的化合物当中,他们分离出一种化合物并且确定了它的结构。他们发现它具有与源自链霉菌的其他药物完全不同的结构。
Zhao说,这些新的化合物可能导致人们开发出新的药物来避免抗生素耐药性或从不同的角度抵抗癌症。
他说,“抗菌素耐药性是一项全球挑战。我们想要发现新的作用机制和新性质,因此我们能够发现新的方法来攻击癌症或病原体。我们想要鉴定出新的化学物骨架来开发新的药物,而不是修饰现存的药物。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎个人转发,网站转载请注明来源“生物谷”,商业授权请联系我们 。更多资讯请下载 生物谷 app.
原始出处:
Mingzi M Zhang, Fong Tian Wong, Yajie Wang et al. CRISPR–Cas9 strategy for activation of silent Streptomyces biosynthetic gene clusters. Nature Chemical Biology, Published online 10 April 2017, doi:10.1038/nchembio.2341

2017年4月12日/生物谷BIOON/—在一项新的研究中,来自韩国基础科学研究所(Institute for Basic Science, IBS)基因组工程中心的研究人员证实了一种近期开发的基因编辑方法的准确性。这种基因编辑工具起着“DNA剪刀”的作用,旨在鉴定和替换人基因组(大小为30亿个碱基对)中的仅一个核苷酸(或者说碱基)。这是首次在全基因组水平上验证了这种“碱基编辑器(base editor)”的准确性。这种验证将有助扩大这种方法在农业、牲畜和基因疗法中的应用。相关研究结果于2017年4月10日在线发表在Nature Biotechnology期刊上,论文标题为“Genome-wide target specificities of CRISPR RNA-guided programmable deaminases”。论文通信作者为来自IBS基因组工程中心的Seuk-Min Ryu和Jin-Soo Kim。
基因编辑工具取得的快速进展已在生物界引起了很大轰动。一种主要的第三代DNA编辑技术是CRISPR。通过切除一小段DNA序列,CRISPR-Cas9和CRISPR-Cpf1被用来沉默或降低有缺陷的基因的表达。然而,去年,生物学家们已发现一种新的碱基编辑器并不导致随机的DNA删除和插入,而是仅替换一个DNA碱基。这种基因校正是至关重要的,这是因为几种疾病是由这四种DNA碱基(即腺嘌呤,简称A;胞嘧啶,简称C;鸟嘌呤,简称G;胸腺嘧啶,简称T)中的一种发生拼写错误导致的。DNA中的单核苷酸错误被称作点突变。点突变导致的疾病包括囊性纤维化、镰状细胞性贫血和色盲。
不同于现存技术的是,在这种碱基编辑器中,CRISPR-Cas9的一种变体(nCas9, 切口酶)与胞嘧啶脱氨酶(cytosine deaminase)APOBEC1融合在一起。APOBEC1将DNA中的碱基C替换为碱基T。这种DNA剪刀被向导RNA(gRNA)引导到DNA上的正确位点。然而,在此之前,人们并不知道这种碱基编辑器是否仅在有缺陷的基因区域上发挥作用,或者它是否在脱靶位点不必要地将碱基C替换为碱基T。
仅一个月之前,Kim团队就在Nature Biotechnology期刊上报道首次成功地在小鼠体内进行单碱基编辑(Nature Biotechnology, doi:10.1038/nbt.3816,相关新闻参见“Nat Biotechnol:首次利用CRISPR培育出单核苷酸编辑转基因小鼠”)。如今,该团队在全基因组水平上证实了这种方法的准确性。
为了鉴定这种方法的可靠性,Kim团队对一种被称作Digenome-seq的错误校验技术进行改进,以便让它适用于这种碱基编辑器方法。去年,当该团队分析了CRISPR-Cpf1和CRISPR-Cas9的准确性时,他们就使用和验证了Digenome-seq。他们也改进了计算机程序Digenome 2.0以便更加全面地鉴定脱靶位点,并且通过比较不同的gRNA发现降低脱靶编辑和增加特异性的gRNA。
利用这种技术,Kim团队发现这种碱基编辑器要比当前的第三代基因编辑工具CRISPR-Cas9更加准确。这种碱基编辑技术在人基因组上的多个位点诱导C→T转换,而CRISPR-Cas9在多个位点上进行切割,这意味着这种新的碱基编辑器产生更少的脱靶变化。Kim说,“因此,我们预计这种碱基编辑器将被广泛地作为一种流行的CRISPR技术加以使用。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎个人转发,网站转载请注明来源“生物谷”,商业授权请联系我们 。更多资讯请下载 生物谷 app.
原始出处:
Daesik Kim, Kayeong Lim, Sang-Tae Kim et al. Genome-wide target specificities of CRISPR RNA-guided programmable deaminases. Nature Biotechnology, Published online 10 April 2017, doi:10.1038/nbt.3852

相关会议推荐

2017(第四届)基因编辑与临床应用研讨会
会议时间:2017.6.9 -6.10 会议地点:上海
会议详情: http://meeting.bioon.com/2017geneediting/?__token=bpc-zixundibu
相关会议推荐

2017(第四届)基因编辑与临床应用研讨会
会议时间:2017.6.9 -6.10 会议地点:上海
会议详情: http://meeting.bioon.com/2017geneediting/?__token=bpc-zixundibu
英国研究人员最新合成出一种人造病毒结构,直径远远小于现有的人造病毒及天然病毒,有望在基因治疗领域发挥实用价值。英国国家物理实验室等机构研究人员在最新一期《美国化学学会杂志》上报告说,这项研究的主要特点在于,研究人员在合成这种人造病毒结构过程中,没有使用大型且结构复杂的蛋白质来制作病毒结构外壳,而是以非常短小的蛋白质“碎片”来拼装。

据英国国家物理实验室介绍,这种人造病毒结构的直径只有12纳米(1纳米等于10亿分之一米),是全球已知病毒中体积最小的一个。此外,这种人造病毒结构比较有可塑性,能够灵活地适应包裹不同大小的基因。
研究人员说,未来可以将这种人造病毒结构当成一个载体,将大小不一的基因包裹其中,从而安全地将基因运送到人体细胞中,且不产生副作用。
基因治疗是一种新兴医疗技术,是指将外源正常基因导入目标细胞,以纠正或补偿基因缺陷和异常引起的疾病。病毒自身不能复制,当接触到宿主细胞时就脱去其蛋白质外壳,将自己的遗传物质注入宿主细胞内。近年来,研究人员希望通过模拟病毒感染宿主细胞的方式,用人造病毒结构作为载体进行基因治疗。(生物谷Bioon.com)
2016年9月22日,位于大鹏新区的深圳国家基因库正式开业。据悉,深圳国家基因库的数据库数据库、样本库、活体库,以及规划数据能力均已超越了EMBL(uropean Molecular Biology Laboratory )、NCBI(Cambridge,UK. GenBank )以及DDBJ(DNAData Base of Japan)世界三大数据库,综合能力位列世界第一,同期,2016年深圳国际BT领袖峰会也在深圳福田开幕,基因库、基因测序已然成为深圳市的亮点产业。
现在,精准医疗已经成为全民热词,在精准医疗中扮演重要角色的测序技术更是深得资本市场、国家政策的青睐,发展日新月异,给医疗科技的创新和产业化带来更多契机。BT领袖峰会基因测序产业发展分论坛上,国内外多名资深专家齐聚一堂,从技术、产业、资本应用的角度探讨下一代基因测序产业的发展。
技术:三代测序异军突起
测序行业发展更代非常迅速:NGS已经成为主流,而一代测序由于其通量有限,但精确度高仍然占据部分市场,而最新的三代技术–无需PCR扩增的单分子测序技术也已问世,目前,拥有单分子测序技术的公司有Helicos Biosciences(美国)、Pacific Biosciences(美国)和Oxford Nanopore(英国),其中只有Pacific Biosciences于2015年10月份推出小型化的单分子测序仪Sequel。

深圳市瀚海基因生物科技公司首席技术官向国兵博士介绍了其公司最新的三代测序技术。据悉,向国兵博士是本月才刚刚加盟深圳瀚海基因,任首席科学家,向国兵博士在回国之前是在美国赛默飞公司任资深科学家,在测序仪领域有超过20年的研发经验,目前全球有超过20%的测序仪正在使用向博士研发的测序试剂,拥有超过50项专利。
向博士介绍说,相比二代测序把基因组减成小段,放大信号的过程,三代测序更为简便,不用扩增,可以进行单分子测序。现在市场上的单分子测序技术有的错误率还有10%左右,”我们瀚海在用的测序技术精确度基本上可以达到百分之百”向博士说。
瀚海的单分子靶向测序有两个比较主要的技术。一是单分子测试,单分子率可以达到60%到70%,已经处于先进水平,同时瀚海研发的新试剂可以帮助单分子成像,在nucleotides里面时可以是自然的链状,第一轮测试完后则可以去掉,不会影响下一轮测试;二是光学方面的全内反射荧光成像(TIRF)技术,TIRF技术中的绿光可以定位,红光用于测序,测完一轮后剪掉,再做另外一个反应。该测序仪一次成像大约有4万个点,通量非常大。
产业:成本下降带来机遇
相比第一代测序来说,下一代测序技术(NGS)最大的突破就在于通量的急剧提升,伴随而来的是测序成本出现几何级的下降,这个规律已经远远超过了IT领域的摩尔定律。16年前为完成中国1%的国际人类基因组任务而成立的华大基因也已经成为中国测序行业巨搫。一个人的基因测序成本也从30亿美金降到今天的1000美金,基因研究也从基础研究逐步走向医学、农业等很多领域。

以医学检测服务为例,华大基因检测涵盖到三个方面,婚、孕、移植前的检测;产前的检测;新生儿的检测。中国每年大概有1700万的新生儿,每年5.6%的出生缺陷率,大概有7000种遗传病,最常见的”唐氏综合症”中国每年有新发病例多达2300多个。国家为了应对这个问题,设计了三级预防体系,分别在在婚、育前阶段、产前阶段和新生儿阶段三个不同的阶段能把出生缺陷的比例控制下去。
在婚前阶段,华大基因设计了一个针对普通人群的遗传病的筛查,包括各个遗传病,尤其是致死、致残率比较高的遗传病。在辅助生殖领域,主要是胚胎植入前遗传学筛查(PGS)和种植前基因诊断(PGD),可以通过二代测序技术,在这两个领域检出在植入前常见的染色体的非整倍体大片段的缺失或者是重复,甚至做一些PGD,可以筛选出健康的胚胎进行植入。在产前阶段,华大提供新生儿代谢病检查服务,新生儿阶段华大提供耳聋的基因检测服务。
随着测序技术的发展,尤其是成本的下降,未来像无创产前检测(NIPT)检测的成本也会逐年的下降,”我们预计到2026年的时候,能够超过95%以上的孕妇,仅仅这一项检测技术,未来的市场规模可能就接近100个亿,所以这项检测技术仍然具有很大的发展空间。”深圳华大基因副总裁和首席市场官赵立见说。
资本:风投融资指数增长
今年是资本的寒冬,有很多热点,比如O2O、大数据的项目等已经很难拿到新一轮融资了,但在医疗健康方向,特别是精准医学方向,近期的投资案例特别多,这是大部分机构或者资本选择的过冬的方式。”医疗健康抗经济下行风险能力是最强的。”澳银资本创始合伙人刘宇先生说。

“当时我们谈的时候,第一轮最多就是五六千万的估值,现在我看到大家纷纷是拿的五六个亿的估值。”刘宇回忆道,在一年前,刘宇团队判断基因检测迎来了一个快速增长期,从国内市场来看都是成倍增长,全球市场2011、2015、2018年的增长速度惊人,特别是与新生儿有关的遗传病等产前筛查的市场已经相对成熟,有华大、贝瑞等企业跑马圈地,跟各地的医院或者是卫计委合作,已经没有太大投资机会了。
在整个市场结构里肿瘤应用占到很大比例,”现在大家普遍看好的肿瘤的早期诊断,个性化的应用,包括预后的指导,可以看到近期的很多案子都是围绕这个发生的。”刘宇评论说。但刘宇也指出,这个行业很火,但也要看到一些风险,基因检测、精准医学有很多的团队,他们是生物背景的出身,跟临床医学中间有一个很大的鸿沟,所以当其真正和医学临床结合时也会面临更多挑战,像华大的平台足够大,可以找到更好的资源、人才去弥补,而大部分的小团队却并不具有这个能力来弥合鸿沟。所以,类似这些投资时间的契机是非常重要的,对投资人而言,如果过早投入,公司没有出里程碑式进展,就没有投资逻辑作支撑,拿不到下轮融资,先驱也就成了先烈。
从基因测序行业角度来看,行业的前景,应用方向是创投机构看重的方向,从逻辑角度来看,投资风险点,是否有相应的增值服务和风险措施手段是创投机构关注的重点。但总体而言,这个行业还是在发展的早期,需要创投的大力支持,但是也需要创业投资资本和投资创业团队之间更好的结合。(生物谷 Bioon.com)
相关会议推荐

2016(第三届)下一代测序发展论坛
会议时间:2016.11.17-2016.11.18 会议地点:上海