2016年12月10日/生物谷BIOON/—CRISPR/Cas9基因组编辑正快速地引发生物医学研究变革,但是这种新技术迄今为止并不是非常精确的。这种技术能够在基因组中无意地产生过多的或者不想要的变化,产生脱靶突变,从而限制了它在治疗应用中的安全性和疗效。
如今,在一项新的研究中,来自美国马萨诸塞大学医学院和加拿大多伦多大学的研究人员发现首批已知的CRISPR/Cas9活性“关闭开关”,从而为CRISPR/Cas9编辑提供更好的控制。相关研究结果于2016年12月8日在线发表在Cell期刊上,论文标题为“Naturally Occurring Off-Switches for CRISPR-Cas9”。
马萨诸塞大学医学院RNA治疗研究所教授Erik J. Sontheimer博士、多伦多大学分子遗传学教授Alan Davidson博士和多伦多大学生物化学助理教授Karen Maxwell博士鉴定出三种自然产生的抑制Cas9核酸酶的蛋白。这些被称作抗CRISPR的蛋白具有阻断Cas9切割DNA的能力。
Sontheimer博士说,“CRISPR/Cas9是一种好东西,这是因为它会引入特异性的染色体断裂从而能够被用来进行基因组编辑,但是鉴于染色体也会是有害的,好东西过多或者让它持续太长时间有可能会适得其反。当前,一旦Cas9被转运到细胞中,就缺乏一种关闭它的可靠方法。如果在执行正确的编辑后,你能够启动关闭开关,那么这种问题就会被解除。我们报道首批已知的Cas9活性的天然抑制剂。”
Davidson博士说,“CRISPR是非常强大的,但是必须能够关闭它。这是对现有工具箱的一次非常重要的补充,这应当给予科学家们更多的信心进行基因编辑。”
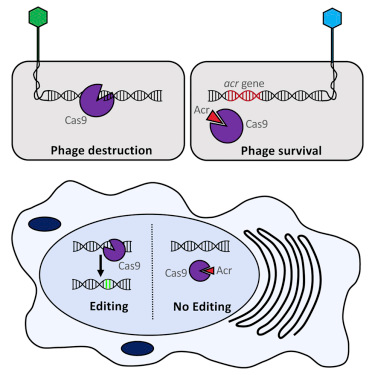
CRISPR/Cas9系统是一种被细菌用来自我抵抗外源遗传物质的适应性免疫系统。它由两个组分组成:一种高效地切割DNA的分子手术刀(Cas9)和一种引导Cas9在精确的位点进行切割的向导RNA复合体(gRNA)。这些gRNA是由含有过去的病毒感染遗留在宿主基因组中的序列片段的CRISPR阵列产生的。通过让Cas9靶向和灭活这些病毒,CRISPR/Cas9系统为细菌细胞提供一种适应性免疫防御。
科学家们能够利用人工gRNA对CRISPR/Cas9系统进行重编程来对哺乳动物基因中的序列进行切割,并且能够让新的遗传信息片段准确地插入到细胞中。作为一种简单而又高效地编辑基因组的方法,CRISPR/Cas9通过让用于研究的细胞系中的基因失活或编辑更加容易而正在改变着生物医学研究。它也让构建能够被用来研究人类疾病的动物疾病模型简单化。过去需要几个月或几年完成的研究工作如今能够在几周内完成。
尽管CRISPR/Cas9系统非常强大,但是它并不是精确的。用来将Cas9引导到基因组中合适位置的gRNA有时候也会引导Cas9到其他类似的但不是相同的序列上。这些错配的位点有时能够被切割,从而导致不想要的损伤。
在很多CRISPR/Cas9应用—包括用于治疗开发—中,存在正被靶向编辑的特定细胞类型、组织或器官,这是因为疾病是在那里自我体现出来或者治疗益处能够在那里实现。
Sontheimer博士说,“在这些情形中,CRISPR/Cas9可能进入目的细胞,但是它也可能进入其他的辅助细胞、组织或器官。Cas9活性在这些辅助细胞、组织或器官中最好是无用的,不然会存在安全风险。但是如果你能够构建出一种让Cas9在除靶组织之外的其他地方保持在非活性状态的关闭开关,那么这种组织特异性将会得到改善。”
Sontheimer博士说,这项新研究不仅鉴定出这种“关闭开关”,而且它还证实Cas9抑制剂自然地存在,而且能够被鉴定出和使用。
他说,“存在很多种不同细菌产生的不同类型的Cas9,而且这些不同的Cas9在基因组编辑中存在着不同的有用性质。已有几种存在于工具箱中的Cas9,而且还会有更多的Cas9出现。我们如今证实这些抑制剂存在自然世界中,而且我们已提供一种可能能够发现它们的策略。”(生物谷 Bioon.com)
本文系生物谷原创编译整理,欢迎转载!点击 获取授权 。更多资讯请下载生物谷APP。
Naturally Occurring Off-Switches for CRISPR-Cas9
April Pawluk, Nadia Amrani, Yan Zhang, Bianca Garcia, Yurima Hidalgo-Reyes, Jooyoung Lee, Alireza Edraki, Megha Shah, Erik J. Sontheimer, Karen L. Maxwell, Alan R. Davidson
 基因君官网
基因君官网
























