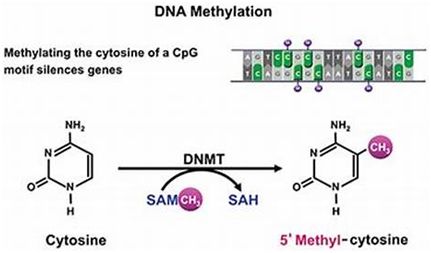
近两年来,以免疫检查点为药物靶点的免疫检查点抑制剂治疗癌症受到越来越多科研工作者的青睐。但是临床研究结果表明,许多癌症患者因接受免疫药物治疗而出现不同程度的免疫相关不良反应,最终出现不得不提前终止治疗的情况。
而寄居在人体内的肠道菌群可以影响免疫检查点抑制剂治疗癌症,能够极大地改善患者对该疗法的响应程度,肠道菌群因其与宿主的共生关系正受到越来越多科研工作者的关注。
2月11日,顶级学术期刊《自然》重磅发布人类肠道菌基因组最新图谱。来自欧洲生物信息研究所(EMBL-EBI)和英国桑格研究所的科学家们最新发现了1952种人体肠道菌,而这些菌种尚未在实验室中进行培养。
这项研究强调,全世界不同人群肠道菌群组成有所不同,通过多样性的样本得出的结果具有非常重大的意义。尽管科学家们已经越来越多详尽的掌握了北美以及欧洲人常见肠道菌群的种类,但是对于全球其他地区的肠道菌群数据却相当缺乏。
人体肠道是许多微生物的家园,这些微生物被统称为肠道菌群。尽管科学家们在肠道菌群领域开展了广泛的研究,但是仍有许多肠道菌无法鉴别,或者其在人体健康中发挥的作用无法确认。导致这种情况的原因有很多,比如这种肠道菌在肠道中的丰度较低或者无法在肠道外环境存活。但是,在这项研究中,科学家们通过计算方法重建这些肠道菌的基因组。他们基于宏基因组学的方法,利用一系列计算工具补充和指导实验室工作,探索人体肠道菌群。
多样化数据收集,新发现1952种人体肠道菌
这些计算方法有效的帮助他们了解在试验中无法培养的细菌。通过对全世界人群的样本进行分析,研究人员又发现了1952种人体肠道菌,使得其谱系多样性增加281%!
研究人员发现,北美和欧洲人群具有大量相同的肠道微生物菌种。然而,少数南美和非洲人群的数据集却出现了前两种人群所不具有显着的多样化特征。这表明,如果科学家们想要真正全面了解人体肠道菌群的组成,对未得到充分代表人群的数据进行收集也是至关重要的。
研究使用的分析方法具有高度可重复性,并且可用于未来更大、更多样化的数据集分析,使得进一步的探索成为可能。研究人员强调,这样的研究正在帮助我们创造一个所谓的人体肠道蓝图,未来可以帮助我们更好地了解人类健康和疾病,甚至可以用于指导胃肠道疾病的诊断和治疗。
人类肠道菌群基因组图谱的研究意义重大,原因之一是肠道菌群的发现与癌症的治疗息息相关。我们知道,目前治疗癌症的方法普遍存在治愈率不高等特点。因此,开辟新的治疗方式十分必要。而肠道菌群能够改善免疫检查点抑制剂治疗癌症引起的不良反应,为癌症的治疗带来了新的曙光。
被忽略的事实,肠道菌群与癌症息息相关
虽然微生物与免疫疗法最近几年才火起来,但是肠道菌群和癌症之间的研究由来已久。1990年就有专家发现幽门螺杆菌和胃癌相关,从那以后,越来越多的其他肠道菌与癌症的发生和发展联系起来。其中一些肠道菌激活炎症反应,破坏保护人体免受外来物质入侵的粘液层,创造了支持肿瘤生长的环境;另有一些肠道菌群通过提高癌细胞对抗癌药物的耐药性促进癌症的生存和生长。
但是肠道菌群同样也可以帮助对抗肿瘤。2013年Laurence Zitvogel教授的一项研究表明,一些癌症治疗方法通过肠道菌群激活免疫系统发挥作用。研究人员发现化疗药环磷酰胺破环了肠道的粘液层,使得一些肠道菌得以进入淋巴结和脾脏,并在这些部位激活特异性免疫细胞。对于实验室中培养的胃肠道内不含有任何肠道菌群的小鼠,或是用抗生素杀灭肠道菌群的小鼠而言,这些抗癌药物则在很大程度上失去了作用。
免疫疗法药物——免疫检查点抑制剂,通常为细胞表面分子(如CTLA4和PD1)抗体,能激发人体免疫系统对抗肿瘤细胞,且被用于多种癌症的治疗(见下图)。但仅20%—40%的患者对免疫检查点抑制剂治疗有反应。
免疫检查点抑制剂作用机制
2015年,Laurence Zitvogel教授团队的研究人员发现,体内无肠道菌群的小鼠对免疫治疗药物无应答,而在注入特定的肠道菌——脆弱类杆菌后,治疗出现了应答。
同样的,Thomas Gajewski教授发现,双歧杆菌可增加小鼠对癌症免疫治疗的反应。通过激发一些免疫细胞的抗瘤能力,双歧杆菌能提高肿瘤的免疫治疗效果。
去年11月,J. A. Wargo教授与Thomas Gajewski、Laurence Zitvogel教授联合在Science上发表论文,通过收集皮肤癌患者免疫治疗的粪便样本进行分析,最后结果指出,免疫疗法治疗效果阳性,与这些患者体内特定种类的肠道菌群有关。曾服用抗生素治疗无关感染的患者往往对免疫治疗反应不佳。
为确认这种关系,研究人员将患者体内的肠道菌群移植到患有同种肿瘤的小鼠体内,与移植免疫治疗反应不佳患者体内菌群的小鼠相比,移植有益菌群的小鼠治疗效果更好,肿瘤出现缩小。
微生物联合免疫疗法,或成抗癌组合拳!
在2015年,有些临床肿瘤学专家一家又一家医院地搜集癌症治疗患者的粪便样本,当时除了一般人会嘲笑外,就连同行的其他医师都会嗤之以鼻。但是,随着近年来相关研究的公布:某些肠道菌可能提高癌症治疗效果,这种嘲讽终于停止了。现在许多肿瘤医师都热衷于分析患者的粪便样本,希望通过这种方法判断抗癌药是否对患者产生作用。这对于不清楚肠道菌和癌症之间的关系的人来说可以说是大开眼界了。
在过去的几十年间,研究人员已经逐渐把肠道菌群与许多疾病联系起来,包括抑郁症、肥胖症等。直至研究人员发现,肠道菌群似乎和癌症也相关,免疫抑制剂的面世让研究者得以进一步的观察肠道菌群和癌症治疗之间的影响,并且可以利用这种影响加强疗效。
在小鼠和人类中的初步研究显示,肠道菌群会对免疫疗法药物产生重要影响,于是研究人员开始尝试解释其中发生的内在机制。目前,研究人员正在启动一部分试验,希望能给通过控制肠道菌群从而改善患者的临床预后。
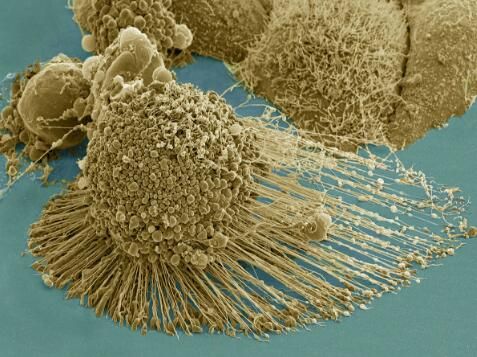
电镜下人类粪便中的菌群,其中有50%来源于肠道
粪便菌群移植,如火如荼走向临床
目前,美国宾夕法尼亚的Hassane Zarour教授正在和全球制药公司Merck开展合作,收集免疫检查点抑制剂治疗反应良好的患者的粪便菌群,并将这些菌群移植到反应性差的患者的肠道内,这项试验将在未来几周内启动。
美国休斯顿的J. A. Wargo教授也在计划着类似的试验,她将与生物技术公司Seres Therapeutics合作,通过粪便菌群移植重塑癌症治疗药物反应性差患者体内的肠道微生物菌群。
美国芝加哥的Thomas Gajewski教授正在和生物技术公司Evelo Biosciences合作,将细菌菌株做成药丸的形式,每种药丸仅含单独一种细菌菌株。他们正在开展临床试验评估含有单一细菌菌株的两种药丸对不同类型癌症患者(包括结肠癌和皮肤癌)的影响。此外,Laurence Zitvogel教授正在研发一种微生物菌群药丸。
目前尚不清楚肠道菌群如何与免疫治疗药物发生相互作用。普遍假设认为,肠道菌群通过调节免疫系统容易被激发的程度来增强人体的抗肿瘤反应。但是确切的机制,包括究竟是哪些菌群调节免疫细胞,目前仍不得而知。希望临床试验将有助于澄清事实。(生物谷Bioon.com)

小编推荐会议 2019(第五届)肠道微生态与健康国际研讨会
http://meeting.bioon.com/2019MicIntestin ?__token=liaodefeng
 基因君官网
基因君官网