
2019年10月13日讯/生物谷BIOON/—尽管CRISPR技术允许对基因组进行更好的操纵,并对现代药物开发和更好的新型抗生素的发现产生许多积极影响,但是当使用该技术时,仍然存在诸如基因组不稳定和Cas9蛋白毒性等重大问题。
不过,在一项新的研究中,来自丹麦技术大学的研究人员开发出一种称为CRISPR-BEST的新工具,它有望成为CRISPR工具箱中的新成员。这种工具可以在不需要引入DNA双链断裂的情况下高效地在放线菌中产生突变。相关研究结果近期发表在PNAS期刊上,论文标题为“Highly efficient DSB-free base editing for streptomycetes with CRISPR-BEST”。
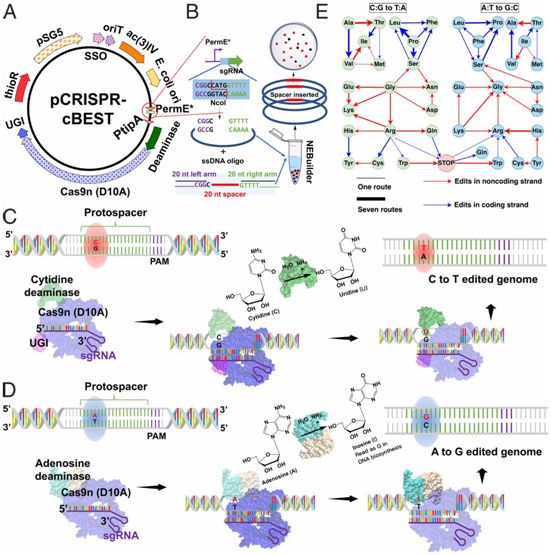
因此,CRISPR-BEST系统解决了放线菌基因工程所面临的一项重大挑战,这是因为引入DNA双链断裂经常导致基因组不稳定,这就迫使放线菌发生重排,或者甚至剔除较大的染色体片段—这是当对细胞进行基因改造以便产生物活性化合物和新型抗生素时想要避免的一种现象。
论文第一作者、丹麦技术大学诺和诺德基金会生物可持续性研究中心研究员Yaojun Tong说,“CRISPR-BEST解决了与当前CRISPR技术相关的一些主要问题。这可能是朝更好地利用诸如基因操纵和基因编辑之类的生物技术的潜力而迈出的一大步。”
两全其美
开发CRISPR-BEST的想法来自于这些研究人员想要使用常规的CRISPR方法来让一个特定基因失活以便产生抗生素黄色霉素(kirromycin)的新变体。但是,在这些实验中,他们丢失了细菌染色体的绝大部分—总共丢失了130万个碱基对,而不是仅让所需的基因失活,而且这种染色体大片段丢失可能是CRISPR切割染色体所导致的。因此,他们开始寻找提高CRISPR编辑效率但同时避免切割染色体的方法。
为此,他们开发出CRISPR-BEST系统。他们认为CRISPR-BEST是实现这种两全其美的一次成功尝试。
论文通讯作者、丹麦技术大学诺和诺德基金会生物可持续性研究中心的Tilmann Weber教授说,“我们维持了CRISPR的编辑效率,这允许我们能够非常容易地靶向感兴趣的基因。但是,在另一方面,我们如今能使用非常温和的条件来引入突变,所引入的突变将给细胞带来更少的压力,因而避免了我们构建出的产生抗生素的细菌出现基因组不稳定的问题。”
进一步优化
CRISPR-BEST是朝着正确方向迈出的重要第一步,不过这些研究人员目前正在研究如何进一步提高编辑效率并增加可以同时进行的基因组编辑数量。这些技术进展可能与使用可以处理大量样本的机器人携手并进,这将为在未来进行大量基因组编辑铺平了道路。
Tong说,“放线菌是抗生素和其他生物活性化合物的最佳生产者之一。对放线菌系统性代谢工程而言,仅有少量基因工具具有统性代谢工程方法所需的高通量和可扩展性—因此仅凭我们如今有了一种新工具的这一事实而言,这已经就是一个优势。”(生物谷 Bioon.com)
参考资料:
1.Yaojun Tong et al. Highly efficient DSB-free base editing for streptomycetes with CRISPR-BEST. PNAS, 2019, doi:10.1073/pnas.1913493116.
2.CRISPR-BEST prevents genome instability
https://phys.org/news/2019-10-crispr-best-genome-instability.html
日前,科技日报记者从获悉,《中国肿瘤基因图谱计划》肺癌课题项目启动。
该课题负责人首都医科大学肺癌诊疗中心主任、教授支修益介绍,《中国肿瘤基因图谱计划》由国家人类遗传资源中心组织,由具有肿瘤单病种临床诊疗特色的医院与高新技术企业共同协作,共同绘制中国肺癌基因图谱,为建立标准化的肿瘤多基因检测提供科学依据。
支修益表示,为达到基于精准医疗的肿瘤早诊早治,需要切实响应《“健康中国2030”规划纲要》、研发新的药物和新的技术,收集中国人群验证数据。《中国肿瘤基因图谱计划》是“健康中国2030”的品牌项目,可以为我国肺癌防控提供精准医学的数据支持,在《中国肿瘤基因图谱计划》课题项目的要求之下,参与中心如何围绕这个项目开展工作,对于促进学科进步发展,中青年医师的培养与发展,提高科室临床、科研相关工作水平具有重要意义,同时参与医院需要与相关学会、协会加强合作,为落实《“健康中国2030”规划纲要》这一目标共同努力。
国家卫健委科学技术研究所/国家人类遗传资源中心主任高华方主任,《中国肿瘤基因图谱计划》是由国家人类遗传资源中心组织,依托国家人类遗传资源共享服务平台,在全国范围内开展人类遗传资源共享及整合的相关工作,将邀请全国50余家大型医院参与项目,肺癌课题计划前瞻性招募2500例患者,有望取得重要成果。
《中国肿瘤基因图谱计划》项目顾问北京大学肿瘤医院教授吕有勇介绍,就多基因检测如何更好解决临床问题做了精彩汇报。基于肿瘤基础研究和临床实践面临的挑战,针对癌症基因组水平的高度异质性和临床生物学行为的复杂性,需要反思部分针对癌症的理念并发展新的研究思路与策略。依据对基因突变谱的系统分析,优化出预测肿瘤侵袭、转移和预后的分子标志物组合为进行多中心大样本临床验证提供了基本素材。《中国肿瘤基因图谱计划》把肿瘤基因大数据与临床诊疗数据相结合,将是肿瘤精准诊疗的重要里程碑事件,本项目应用的大Panel多基因检测可以全面囊括肿瘤低频基因突变,辨识肿瘤的高度异质性,从而可以更全面地认知肿瘤,解决临床问题。肺癌治疗领域内近年间已获多项重要成果,相信《中国肿瘤基因图谱计划》可以为肿瘤检测领域带来更多的成果和突破。
作为《中国肿瘤基因图谱计划》肺癌课题项目牵头单位代表,首都医科大学宣武医院胸外科医师钱坤表示,肺癌基因图谱已有相关报道,例如美国的肿瘤基因图谱计划——TCGA项目,但由于东西方人群存在种族差异,导致肺癌基因图谱也会存在着不同,以西方人群为基础的数据库指导中国人群的肿瘤诊疗会有偏差。《中国肿瘤基因图谱计划》肺癌课题将以多中心合作的方式,在全国范围内前瞻性招募2500例肺癌患者,旨在绘制中国肺癌基因图谱,为建立标准化的检测分析流程提供科学依据,探寻中国人群肺癌靶向、免疫治疗疗效、预后分子标志物,有望产出肿瘤领域的高水平文章。(生物谷Bioon.com)
小编推荐会议 2019无锡国际生物医药论坛暨第九届Cell Death & Disease国际研讨会-新药研发
http://meeting.bioon.com/BCDD?__token=liaodefeng

基因组稳定性的维持是一切生命活动的基础,然而,多种外源和内源因素作用下产生的广泛DNA损伤和复制压力构成了基因组不稳定的主要来源。真核生物的生存严格依赖ATR(ataxia telangiectasia–mutated and Rad3-related)激酶的活性,ATR激酶负责启动细胞对基因组不稳定的响应和修复,全局性地调控基因组的稳定,也是细胞内重要的肿瘤抑制因子。
脂肪酸合成酶(fatty acid synthase, FAS)负责催化乙酰CoA和丙二酸单酰CoA合成长链脂肪酸。脂肪酸合成过程中,底物和中间产物分子在FAS各个功能结构域中传递直到完成脂肪酸的整个合成过程。有研究表明,编码FAS的基因可能发挥着癌基因的功能,其表达水平在部分肿瘤细胞中发生上调,利用FAS抑制剂抑制脂肪酸的合成,肿瘤细胞的增殖和扩散也能够明显地受到抑制(Khan et al., 2014; Liu et al., 2010)。
中国科学技术大学蔡刚教授课题组和王雪娟教授课题组在内源性纯化裂殖酵母ATR-ATRIP(Rad3-Rad26)复合体的过程中,很意外地发现Rad3-Rad26可以与FAS一起从体内稳定地共纯化,这个结果暗示着ATR激酶在体内可能通过直接结合FAS调控脂肪酸代谢。阐明ATR与FAS之间的功能性相互作用及其生物学意义,不仅能显着提升对DNA损伤应答通路和脂肪酸合成通路之间联系的认识,也有望为肿瘤治疗提供新的方向。
针对上述科学问题,蔡刚教授和王雪娟教授两个课题组合作在Journal of Molecular Cell Biology(JMCB)发表了题为“Modulation of Fatty Acid Synthase by ATR checkpoint kinase Rad3”的研究成果,揭示裂殖酵母ATR-ATRIP复合体(Rad3-Rad26)稳定地与FAS结合,通过调控FAS的结构柔性,将脂肪酸合成停滞在启动阶段(见上图中步骤2)。
在发现Rad3-Rad26在体内结合FAS的基础上,进一步的工作揭示Rad3-Rad26与FAS的相互作用在体内、外分别受到DNA损伤和饱和脂肪酸的调控。当细胞受到DNA损伤时,Rad3-Rad26与FAS的体内相互作用明显增强;在体外,Rad3-Rad26与FAS的直接结合能力较弱,加入饱和脂肪酸能显着促进其二者的相互作用。随后利用冷冻电镜技术,作者分别解析了单独状态以及Rad3-Rad26共纯化状态下FAS的三维结构。单独的FAS具有高度的结构柔性,底物运输核心ACP(acyl carrier protein)结构域处于连续的构象变化,在各个催化结构域间来回穿梭,具备高速合成脂肪酸的能力;而共纯化FAS的ACP结构域则被铆钉在AT (acetyl transferase)和SD1(structural domain 1)结构域之间,脂肪酸合成被停滞在起始阶段,FAS的合成活性也显着降低。
癌细胞在转移过程中,细胞内营养物质及能量的流通速率往往高于正常细胞。如糖代谢异常活跃、脂肪酸过度累积;而这些代谢的变化能满足癌细胞的粘附、转移和生存的需要。本研究首次发现了ATR激酶与FAS具有直接的相互作用并且能够抑制脂肪酸合成,揭示了ATR激酶除了调控基因组稳定性外,其肿瘤抑制因子的作用还可能通过直接抑制脂肪酸合成来发挥。此外,本文还发现了DNA损伤响应与脂肪酸合成代谢之间存在直接的联系,提供了认识ATR激酶和FAS这两种重要抗癌靶点的全新视角。(生物谷Bioon.com)

近日,清华大学等科研人员在Nature Communications上发表了题为“Oncolytic adenovirus programmed by synthetic gene circuit for cancer immunotherapy”的文章,利用合成基因线路对溶瘤病毒进行编程,提高了溶瘤病毒治疗的特异性,实现了免疫效应子的可控和局部表达,有望成为多种癌症的治疗策略。
溶瘤病毒(oncolytic virus)是一类具有复制能力的肿瘤杀伤型病毒。通过对自然界存在的一些致病力较弱的病毒进行基因改造制成特殊的溶瘤病毒,利用靶细胞中抑癌基因的失活或缺陷从而选择性地感染肿瘤细胞,在其内大量复制并最终摧毁肿瘤细胞。同时它还能激发免疫反应,吸引更多免疫细胞来继续杀死残余癌细胞。与传统药物具有明确的药代动力学和药效学不同,溶瘤病毒免疫治疗的结果依赖于肿瘤细胞、病毒和周围免疫细胞的种群动力学和相互作用,由于难以提高对癌症的特异性和免疫反应,以及对种群动态了解有限,如何提高溶瘤病毒疗法的疗效仍然充满挑战。在本研究中,科研人员构建了一个可控的、模块化的合成基因线路,能够根据不同的启动子和MicroRNA(miRNA)的输入,选择性地控制肝细胞肝癌细胞中腺病毒的复制和免疫效应子(immune effectors)的释放。通过小鼠模型实验和计算机模拟,科研人员发现可复制腺病毒比不可复制腺病毒具有更好的抑瘤效果。在免疫活性小鼠模型中,可以观察到联合肿瘤裂解和免疫调节剂的分泌,对于局部淋巴细胞毒性和系统免疫的提高可以产生协同效应。此外,该研究的计算模拟表明,编码免疫调节剂的溶瘤病毒比溶瘤病毒和免疫效应子的联合治疗有更好的治疗效果。该研究提供了一个有效的溶瘤腺病毒设计方法,有望应用于多种癌症免疫治疗。(生物谷Bioon.com)

2019年12月9日 讯 /生物谷BIOON/ –近日,一项刊登在国际杂志Gastroenterology上的研究报告中,来自罗格斯大学的科学家们通过研究发现,帮助肠道干细胞燃烧膳食脂肪的两个基因或在结肠癌发生过程中扮演关键角色。文章中,研究者阐明了小鼠机体细胞消耗脂肪的方式与基因调节肠道干细胞行为机制之间的关联。

图片来源:Lei Chen
研究者Michael Verzi教授表示,这一点非常重要,因为当肠道中存在太多膳食脂肪时,干细胞的数量就会增加,进而就会增加机体患结肠癌的易感性;人体每天都会失去数百万个肠道细胞,就好比我们失去皮肤细胞一样,肠道干细胞会经历不断地更新和肠道内壁的不断更新,但改变干细胞的功能或会引发结肠癌。
结直肠癌是美国人群中第三大常见的癌症类型,据美国癌症协会数据显示,每年大约有101,420人会被被诊断为结直肠癌患者。最近有研究表明,肠道干细胞的水平会在摄入高脂肪“西方”饮食的动物中增加,这或许就能够解释这种饮食方式增加癌症风险的原因。这项研究中,研究人员发现,HNF4A和HNF4G基因能互相协作来促进肠道内壁保持良好的功能,当这些基因被失活后小鼠就会失去肠道干细胞,这就证实了这两个基因的重要性,此外研究者还认为,这些基因能帮助干细胞燃烧脂肪从而为机体提供能量。
最后研究者表示,我们希望后期能够进行更为深入的研究来阐明在高脂肪饮食期间,HNF4A和HNF4G基因是否能够改变肠道干细胞数量并增加癌症风险。(生物谷Bioon.com)
原始出处:
Lei Chen et al, HNF4 Regulates Fatty Acid Oxidation and is Required for Renewal of Intestinal Stem Cells in Mice, Gastroenterology (2019). DOI: 10.1053/j.gastro.2019.11.031
图片来自:yourgenome.org
2017年9月28日/基因宝jiyinbao.com/— 弗吉尼亚大学医学院( UVA )已经开始为青少年急性淋巴细胞白血病,实施基于基因工程改造的T细胞免疫治疗。 I / II期的青少年急性淋巴细胞白血病试验,正在评估该方法对儿科患者的安全性和有效性。该项临床试验将考察总体缓解率、12个月后缓解期和整体生存期等因素。参与者必须介于2岁和21岁之间,并且要求患者已经复发或对其他形式的治疗没有反应。
被称为嵌合抗原受体(CAR)T细胞疗法的方法是利用人体自己的免疫T细胞,通过基因修饰它们,使它们更有效地杀伤癌细胞。在这种情况下,UVA儿童医院的癌症中心和卡特免疫中心儿科肿瘤学家 Daniel Lee博士,从一名年仅14岁的急性淋巴细胞白血病患者身上抽取T细胞,然后,该患者的免疫细胞由 Kite Pharma 细胞治疗公司进行基因改造。
实验方法类似于美国联邦食品和药物管理局8月底批准用于儿科淋巴细胞白血病的基因疗法,这是美国曾经批准的第一个基因治疗方法, Daniel Lee博士希望该方法将给病人带来希望。“我们从患者的静脉收集T细胞,细胞运送到基因编辑公司,基因改造大约在七天内完成,并将改造后的T细胞返回给我们,”Lee博士说。“所以我们只需要有16到18天的等待时间,这是非常快的。”
在美国国立卫生研究院的时候,Lee博士在50多名试验参与者中使用类似产品来测试该方法。他说,这些参与者对该方法有反应的比例为70%,复发率低于10%。可能在不到两年的时间内,将会陆续有20个临床试验完成。
因为Lee博士在CAR T细胞疗法方向的开创性研究,UVA从NIH招募了Lee博士。除了白血病治疗之外,他还在寻求开发新型的T细胞治疗方法用于挽救致命的儿科脑癌。在UVA,他加入了一个世界级的研究团队,探索免疫治疗的潜力,以提高身体抵御疾病的能力。他说:“你将会看到更多的CAR T细胞治疗法出自UVA。” (生物谷 Bioon.com)
参考资料:
Teen first in Virginia to receive cancer gene therapy in clinical trial
本文中,小编对多篇文章进行整理,让我们一起关注近期全球基因疗法的研究进展。
近日,Spark Therapeutics传来喜讯。美国FDA的一个独立专家小组在经过仔细的审评后,以16:0的投票,对其在研基因疗法Luxturna表示一致认可。这也意味着首款能矫正人类基因缺陷的疗法离我们更近一步。美国FDA将在2018年1月12日前就这款新药能否上市做出批复。
罹患遗传性视网膜病变(IRD)的患者是这款创新疗法的最大受益者,25岁的艾莉森·科罗纳(Allison Corona)就是其中之一。这名年轻的姑娘不幸患有莱伯先天性黑蒙症(Leber congenital amaurosis),很难分清颜色,日常生活中也只能看见人的大致轮廓。辨识对方表情这样简单的任务,对艾莉森来说是个奢望。她说,她的生活缺失了很大一部分。
艾莉森患上的是一种遗传病,背后的根本原因在于关键基因的突变。这些基因对于视网膜的发育和功能有着重要作用,一旦无法正常工作,就会影响到人的视力,导致失明。由于这种疾病的根源在于基因本身,大部分只能“治标”的药物对其无能为力。
doi:10.1073/pnas.1701589114
大部分永久性失明的症状产生都是由于视网膜中数一百万计的光感受体细胞(类似于数码相机的像素点)的缺失导致的。然而,视网膜中那些残余的、对光线敏感度不高的视觉神经细胞则处于正常状态。最近,来自牛津大学的Samantha de Silva等人通过病毒转染的方式在患有“视网膜色素变性(一类常见的导致青少年失明的原因)”的小鼠眼部残余的视神经细胞中表达光感蛋白(melanopsin),从而使得小鼠的视力得到了部分的恢复。
研究者们对这些接受转基因治疗的小鼠进行了长达一年的观察,结果显示,小鼠的视力能够在较长的时间范围内维持正常水平(即小鼠能够对环境中的事物进行辨别)。这类表达有melanopsin的细胞则能够对光线产生反应,以及能够向大脑传送视觉信号。虽然此前牛津大学的研究者们已经通过向患者眼部移植电子视网膜进行治疗,但这种基因疗法显然更加简单。
在这项两年多随访的试验中, 17例脑性肾上腺脑白质营养不良(cALD)的患者使用蓝鸟生物(Bluebird)的单剂量基因疗法Lenti-D治疗, 15例患者的病情得以稳定。
这项发表在《新英格兰医学》杂志上的试验结果表明, Lenti-D可能会是cALD的第一个根治疗法。
cALD是一种罕见病,是肾上腺脑白质营养不良(ALD)中较为严重的一种。据估计全球每2.1万男就有1人患ALD,患ALD的男性中有40%为脑性cALD。
而肾上腺脑白质营养不良(ALD)是一种遗传病,ALD患者因为ABCD1基因的突变导致丧失了肾上腺脑白质营养不良蛋白(ALDP)功能。因为ALDP是超长链脂肪酸(VLCFAs)分解的关键蛋白质,这个蛋白的功能丧失导致血液和所有组织中VLCFAs的有毒性积累,以肾上腺和神经系统的影响最大。
【4】“电子基因疗法”治疗心脏病
新闻阅读:Electric genes hope to fix a broken heart
最近,科学家们开发出了一种新型的”电子基因”疗法,有望为心脏疾病提供革命性的治疗方案。
心脏病是欧洲范围内致死率最高的疾病。仅仅2013年就有190万人因心血管疾病死亡,占据当年死亡总人数的37.5%。
存在较高心脏节律紊乱风险的人群往往会通过手术的方式移植一个心脏除颤器。然而,如果心脏本身就能够检测并且修复自身的紊乱症状的话又当如何呢?这就是来自荷兰Leiden大学医学中心的心脏专家D?niel Pijnappels博士致力于解决的问题。

Voyager Therapeutics公司宣布了评估VY-AADC01治疗晚期帕金森病的1b期临床试验的积极结果。证明了一次性施用这一基因疗法可以对患者运动功能的多项测量起到持久的改善作用。
帕金森病是一种慢性进展性的神经退行性疾病,是由于制造多巴胺的神经元丧失造成的,表现为震颤、运动缓慢、僵硬、姿势不稳定等,发展到晚期甚至引起摔倒、无法迈步、语言和吞咽困难等,需要人照顾日常生活。它影响了全球约700万至1000万人。但目前还没有可以有效延缓或逆转疾病进程的治疗。左旋多巴是标准治疗方法。早期帕金森病患者通常可以通过左旋多巴较好地控制病情,但随着疾病进展,患者对治疗的响应也变得越来越差。据估计,约有15%的帕金森病患者有运动能力波动,并且经左旋多巴治疗不能很好的控制。患者会经历更长时间的运动能力降低(也叫“关闭”期),药物提供的有效时间(也叫“开启”期)会变短。患者急需一种可以有效延缓疾病进程,并缓解症状的疗法。
【6】新疗法:科学家将一种基因工程病毒注入肿瘤以此破坏肿瘤生长!
桑福德健康是美国第一个使用基因工程病毒进行临床试验的网站,旨在破坏耐药性肿瘤。
I期免疫治疗试验适用于18岁及以上患有不符合标准治疗的转移性实体瘤。该治疗将肿瘤溶解性(破坏坏死)的病毒 – 水泡性口炎病毒(VSV)注射入肿瘤。病毒被设计成在癌细胞中生长,破坏这些肿瘤,然后传播到其他癌症部位。在这个过程中,它向该区域招募免疫系统,目的是引发免疫反应。
该病毒,通常称为VSV,可以感染牛,但很少引起人类严重感染。
病毒通过添加两个基因进行遗传改变。第一个基因是人类干扰素β基因,它是一种天然的抗病毒蛋白质。这可以保护正常的健康细胞免受感染,同时仍能使病毒对抗癌细胞。
第二个基因为甲状腺中发现的NIS蛋白质,这使得研究人员可以在病毒传播到肿瘤部位时跟踪病毒。 Vyriad是明尼苏达州罗彻斯特的一家生物制药公司,开发了该技术,由梅奥诊所分子医学教授,溶瘤病毒治疗专家Stephen Russell博士领导。
【7】Cell Stem Cell:重磅!科学家开发出新型经皮肤移植的基因疗法 或能有效治疗多种人类疾病
DOI:10.1016/j.stem.2017.06.016
近日,一项发表在Cell Stem Cell杂志上的一篇研究报告中,来自芝加哥大学的研究人员通过研究克服了限制基因疗法的瓶颈,文章中,研究人员阐明了如何利用皮肤移植的方法来促进基因疗法治疗多种人类疾病。
研究者Xiaoyang Wu博士表示,经过皮肤移植的基因疗法或能帮助有效治疗两种常见的疾病:2型糖尿病和肥胖症;这项研究中,研究人员设计出了具有完整免疫系统的小鼠—小鼠皮肤移植模型,这个平台或能支持在小鼠甚至在人类机体中进行安全和可持久的基因疗法;研究者表示,工程化的皮肤移植或能在完整免疫系统的野生型小鼠中存活时间较长,而且皮肤移植的成功率能够达到80%以上。
研究人员重点对糖尿病进行了相关研究,首先他们插入了编码胰高血糖素样肽1(GLP1)的基因,这种激素能够刺激胰腺分泌胰岛素,额外的胰岛素则会从血液中移除过量的葡萄糖,从而抑制疾病并发症的出现,GLP1也能够减缓胃排空的时间并且降低机体食欲。随后研究人员利用CRISPR工具对GLP1基因进行了修饰,当研究者插入能够延长血液中激素半衰期的突变后,就能够将修饰后的基因同抗体片段融合以便这些抗体能够在血液中循环较长时间。
【8】Nat Commun:基因疗法治愈哺乳动物肌营养不良症
英法合作团队在25日出版的《自然·通讯》杂志发表论文称,他们以狗为动物试验模型开发的基因疗法,成功治好了杜氏肌营养不良症(DMD),为下一步开展人类临床试验铺平了道路,向治愈人类DMD患者迈出重要一步。
DMD患儿均为男性。在新出生的男婴中,每5000人就有一人会患上此病。这些患儿在几岁时就会表现出肌无力症状,如行走缓慢、跑步时容易跌倒、上楼和下蹲困难、走路呈典型鸭步等;一般到15岁之前,会恶化到无法自己行走,依靠轮椅生活;随后各种肌无力、呼吸及心脏问题相继出现,病人很少能活到40岁。
科学家们认为,DMD由一种与抗肌萎缩蛋白有关的基因变异引起,这些基因变异会影响抗肌萎缩蛋白的生成,进而影响肌肉的健康和功能。新研究中,法国南特大学和英国伦敦大学的科学家合作,研发出一种新型基因转移疗法,成功恢复了实验狗体内抗肌萎缩蛋白的表达。

近日,在顶尖学术刊物《细胞》的子刊《Cell Stem Cell》中,来自芝加哥大学的Xiaoyang Wu教授团队发表了他们的一项新发现——将干细胞技术、CRISPR基因编辑技术、与皮肤移植技术相结合,一款基因疗法有望对肥胖症与2型糖尿病这两种常见疾病进行治疗。
自上世纪70年代以来,科学家们就学会了如何从烧伤患者身上分离出皮肤干细胞,在实验室中进行培育,并移植到患者的烧伤部位,进行治疗。这给Wu教授的团队带来了启示。如果我们在这些皮肤细胞中引入能治病的基因,是否就能把皮肤改造成人体的药厂,随时生产能治疗疾病的药物呢?
研究人员决定以小鼠糖尿病为模型检验这个想法。选择糖尿病有几个原因。首先,它的病理与皮肤无关,因此不大可能受皮肤移植的影响。其次,我们知道,用一些简单的蛋白质,就能对糖尿病进行治疗,这便于基因疗法的开发。
日前,位于美国马里兰州(Maryland)的再生医学公司TissueGene宣布,该公司在亚洲(包括韩国)的合作伙伴Kolon Life Science已经从韩国食品医药品安全部(MFDS)获得了Invossa的上市许可,它也是全球首个上市的针对退行性关节炎的细胞和基因疗法。
骨关节炎(osteoarthritis)是最常见的关节炎类型,它产生的主要原因是关节中软骨层受到破坏和耗损,导致软骨下面的骨骼相互摩擦。这导致患者关节疼痛、肿胀和活动范围减小。随着病情的发展,关节可能会变形或长出骨刺。关节腔内浮游的骨骼和软骨碎片可能导致更多疼痛和损伤。目前治疗骨关节炎的常见方法包括口服消炎止痛药,向关节中注射类固醇或透明质酸(hyaluronic acid),以及关节置换手术。这些疗法大多只能暂时减轻疼痛,而关节置换术价格不菲,并且伴随着手术带来的风险。

【11】Cell:重磅!科学家开发出基于CRISPR的新技术 或有望开发更为安全的基因编辑疗法
doi:10.1016/j.cell.2017.05.044
日前,一项刊登在国际著名杂志Cell上的一篇研究报告中,来自美国德克萨斯大学(The University of Texas)的研究人员通过研究利用CRISPR开发出了新型的基因编辑疗法来治疗危及生命的疾病,比如癌症、HIV和亨廷顿氏症等。
如今科学家们能够利用基因魔剪—CRISPR来对几乎任何有机体的遗传代码进行编辑,基于CRISPR的基因编辑技术对人类健康有着巨大的影响,目前已经有一系列利用CRISPR技术对人类细胞进行的试验正在进行之中,但这种方法似乎并不完美;从理论上来讲,基因编辑的工作原理就类似于利用一种自动纠正功能俩修复文档中重复出现的错误,但寻找并且编辑基因的CRISPR蛋白有时候却会靶向作用错误的基因,这样其就会将拼写正确的单次修正为拼写错误的单词,然而对错误的基因进行编辑还会产生新的问题,比如促进健康细胞发生癌变。
文章中,研究人员开发了一种新方法,其能够通过个体的完整基因组来快速检测CRISPR分子,从而预见除了CRISPR的靶点外其是否还能够同其它DNA片段相互作用,这种新方法或许就能够帮助临床医生为患者制定个体化的基因疗法,同时还能够保证疗法的安全性和有效性。Ilya Finkelstein教授说道,你和我之间或许会出现大约100万个点的差异,由于这种遗传多样性的存在,对人类基因的编辑似乎总是一种需要进行定制化的疗法。(生物谷Bioon.com)
生物谷更多精彩盘点!敬请期待!