2017年11月3日/生物谷BIOON/—在一项新的研究中,布罗德癌症依赖性图谱(Broad Cancer Dependency Map)团队将来自342种癌细胞系的基于CRISPR的数据添加到他们不断增加的癌症基因依赖性目录中,并且提供一种新的方法来确保这些数据的准确性。相关研究结果于2017年10月30日在线发表在Nature Genetics期刊上,论文标题为“Computational correction of copy number effect improves specificity of CRISPR–Cas9 essentiality screens in cancer cells”。
基于CRISPR的全基因组敲除筛选是确定细胞基因依赖性—也就是细胞存活和/或增殖所需的基因—的强大工具。然而,这样的CRISPR筛选对一种被称作拷贝数效应(copy number effect)的现象较为敏感。拷贝数效应指的是细胞中重复复制的基因(正如癌细胞中经常发生的那样)不管是不是必需基因,都会被标记为必需基因。
为了限制这些假阳性结果,布罗德癌症依赖性图谱计划—一个将来自布罗德癌症项目的阿喀琉斯计划团队和癌症数据科学团队、布罗德研究所基因扰动平台和其他的布罗德研究所团队的研究人员召集在一起的联合计划—开发出一种被称作CERES的计算方法,该方法可对汇集的CRISPR筛选数据进行拷贝数效应校正,并且针对癌细胞的基因依赖性提供给一种无偏见的看法。
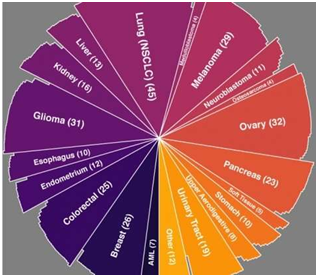
正如布罗德癌症依赖性图谱团队在这项研究中报道的那样,他们利用CERES对来自342种癌细胞系的全基因组CRISPR-Cas9筛选数据(迄今为止产生的最大CRISPR敲除数据集)进行校准,这些癌细胞系是由布罗德-诺华癌细胞系百科全书(Broad-Novartis Cancer Cell Line Encyclopedia, CCLE)进行管理的。这种方法极大地降低这些数据中的假阳性结果,准确地找到了已知的基因依赖性(如KRAS基因突变),并且允许新的基因依赖性浮现出来。
当癌细胞为因突变或表达变化导致至关重要的基因丢失寻找补救措施时,这些新的基因依赖性数据可作为布罗德癌症依赖性图谱团队正在进行的利用CRISPR和RNA干扰(RNAi)等功能性基因组技术确定这些癌细胞中出现的脆弱位点的努力的有力补充。今年早些时候,该团队已宣布他们利用全基因组RNAi筛选列出了769个强大的基因依赖性,这是将近10年努力的成果。
该团队之前开发两种计算方法ATARiS和DEMETER,用于过滤501种CCLE管理的细胞系的功能性基因组筛选数据中的假阳性结果。这两种方法都会清除通常困扰着RNAi数据的所谓的种子效应(seed effects)。CERES则将这两种计算方法结合在一起。(生物谷 Bioon.com)
参考资料:
Robin M Meyers, Jordan G Bryan, James M McFarland et al. Computational correction of copy number effect improves specificity of CRISPR–Cas9 essentiality screens in cancer cells. Nature Genetics, Published online 30 October 2017, doi:10.1038/ng.3984
 基因君官网
基因君官网