2018年7月7日/生物谷BIOON/—CRISPR/Cas基因编辑工具的开发标志着靶向改变遗传信息取得的一次革命性进展。它为基础研究和基因修复提供了大量机会。然而,改变DNA也有风险—它所引起的任何错误将永久性地储存在基因组中,因此可能在较晚的时候给接受DNA改变的个体和他/她的后代带来问题。
德国蒂宾根大学跨学科生物化学研究所的Thorsten Stafforst教授及其团队7年来一直试图开发出一种低风险的替代方法:在RNA水平上进行靶向改变。这种新方法利用一种正常的细胞过程:编码在DNA中的遗传信息经转录后产生RNA,当RNA不再需要时,它便被降解掉。如果改变RNA,那么初始的遗传信息将仍然保留在DNA中。如今,在一项新的研究中,Stafforst团队能够利用这种替代方法精准地和高效地在细胞中编辑这些RNA转录本。相关研究结果发表在2018年7月的Nature Methods期刊上,论文标题为“Efficient and precise editing of endogenous transcripts with SNAP-tagged ADARs”。
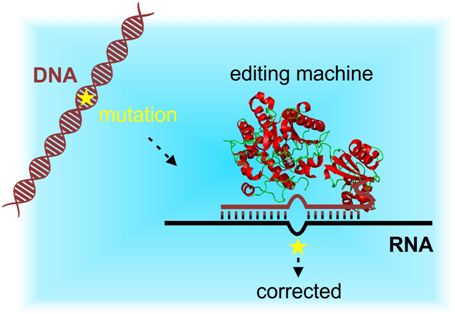
细胞将它的DNA中携带的遗传信息转录为RNA分子。这种遗传信息成为用来产生无数种具有不同组成的蛋白的一组指令。这些蛋白接着作为细胞中的构成单元(building block)发挥作用和控制它的代谢。Stafforst解释道,“我们的RNA编辑方法基于一种蛋白构造体。在一种向导RNA(gRNA)的帮助下,这种蛋白构造体到达到靶RNA分子上,并转化某些碱基。这就使得重写用来产生蛋白的指令成为可能。”RNA操纵能够受到精细调节并且是可逆的,这就使得这种方法在治疗由突变引起的疾病方面特别有吸引力。
具体而言,这种蛋白构造体是通过将作用于RNA上的腺苷酸脱胺酶(adenosine deaminases acting on RNA, ADAR)与SNAP-tag融合在一起而产生的。这种蛋白构造体在gRNA的引导下能够将靶RNA转录本中的腺苷酸(A)转化为肌苷酸(I)。Stafforst团队利用这种蛋白蛋白构造体同时对两种疾病相关的编码信号蛋白的RNA转录本KRAS和STAT1进行高效地编辑。
限时操纵RNA
Stafforst指出这种工具可能能够编辑多种引起疾病的突变。他补充说,RNA中引入的瞬时变化使得干预信号通路(比如与炎症有关的信号通路)成为可能,这是因为永久性操纵RNA有可能会产生严重后果。Stafforst说,“我们已证实这种方法能够同时编辑多种编码信号蛋白的RNA转录本。”Stafforst团队证实他们的方法的编辑效率是近期公布的基于一种CRISPR/Cas变体的定点RNA编辑方法(即Cas13b–ADAR)的2倍。
通过与美国斯坦福大学的Jin Billy Li教授及其团队合作,Stafforst团队证实这种方法仅会产生少量错误,而且他们能够将这些错误降到最低。Stafforst补充道,这种方法是高效的,而且比其他的编辑方法具有更高的特异性。
将定点RNA编辑用于基础研究和医学的研究工作才刚刚开始。Stafforst说,“未来,我们想要放弃经过基因改造的蛋白,转而使用天然存在的酶来进行定点RNA编辑。”Stafforst团队已就他们开发出的这种方法申请了专利。(生物谷 Bioon.com)
参考资料:
Paul Vogel, Matin Moschref, Qin Li et al. Efficient and precise editing of endogenous transcripts with SNAP-tagged ADARs. Nature Methods, July 2018, 15(7):535–538, doi:10.1038/s41592-018-0017-z
 基因君官网
基因君官网