2018年10月14日/生物谷BIOON/—大多数哺乳动物细胞含有一个细胞核,这个细胞核中容纳的DNA如果拉成直线的话则长6英尺以上。这种遗传物质决定着细胞的命运,而且如果它处于不合适的位置或者遭受损伤的话,那么它能够导致疾病。之前的研究已表明DNA倾向于在细胞核的某些区域聚集在一起。然而,这种放置如何影响DNA的功能仍然是不清楚的。
在一项新的研究中,来自美国斯坦福大学的研究人员通过解除CRISPR-Cas9的“切割”功能,这种编辑工具变得更像是一种递送系统,这样就能够通过可编程的向导RNA(gRNA)将DNA片段递送到细胞核中的新位置上。这种称为CRISPR-基因组组装(CRISPR-genome organization, CRISPR-GO)的新技术使用一种经过修饰的CRISPR蛋白,从而在三维空间中重新组装基因组。如果CRISPR-Cas9像分子剪刀一样,那么CRISPR-GO就像分子镊子一样,抓住基因组中的特定部分,并且将它们放置在细胞核的新位置上。但是这并不仅仅是物理上的重新安置:改变DNA片段的位置能够改变它们的运作方式。相关研究结果于2018年10月11日在线发表在Cell期刊上,论文标题为“CRISPR-Mediated Programmable 3D Genome Positioning and Nuclear Organization”。论文通信作者为斯坦福大学化学与系统生物学助理教授Lei S. Qi博士。
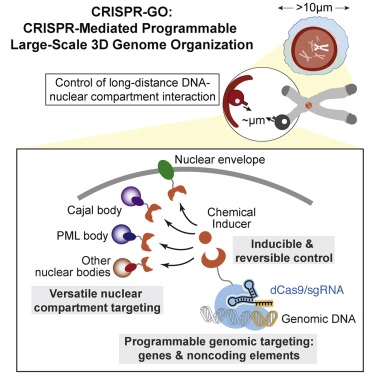
CRISPR-GO有三个基本部分。首先,你想要重新定位的靶DNA片段所在的“地址”—一段DNA,它能够靶向一条互补的结合RNA的链。其次,你需要目标地址—你想要将染色质移动到的细胞核区室中的特定DNA部分。最后,还存在“桥(bridge)”,在这种情形下,它是一种催化剂,它促进靶DNA片段移动到它在细胞核中的目标地址。
细胞核中有多个区室,它们在维护细胞功能方面都具有特定的作用。Qi和他的实验室研究了细胞核的三个不同区域,测试他们是否能以某种方式改变染色质的功能,这取决于他们将它移动到何处。
通过使用CRISPR-GO,这些研究人员观察到重新定位到卡哈尔体(Cajal body)—作为细胞核中的一部分,它是一团无定形的且有些神秘的蛋白和RNA —中的基因停止表达蛋白。他们首次有证据证实卡哈尔体能够具有直接的基因调节作用。这提示着卡哈尔体在控制转录方面有一些意想不到的作用。
当Qi利用CRISPR-GO将端粒DNA —染色体上的与长寿相关的分子帽—从细胞核的中间移动到细胞核的边缘时,端粒停止生长,从而阻止细胞周期和降低细胞活力。然而,当端粒更靠近卡哈尔体时,相反的情形发生了:它们生长,并且通过这样做,细胞活力也增加了。
CRISPR-GO的第三种应用是形成早幼粒细胞白血病小体(promyelocytic leukemia body, PML小体)。众所周知,这种蛋白团块抑制促肿瘤基因表达。通过将它放置在细胞核中的致癌基因附近,Qi计划测试它是否能够有助于抑制肿瘤形成。
Qi表示,虽然利用CRISPR-GO提供的证据是令人兴奋的,但是这项研究仍处于试验阶段,在这些研究结果得到验证之前,还有更多的研究工作需要开展。(生物谷 Bioon.com)
参考资料:
Haifeng Wang, Xiaoshu Xu, Cindy M. Nguyen et al. CRISPR-Mediated Programmable 3D Genome Positioning and Nuclear Organization. Cell, Published Online: 11 October 2018,
doi:10.1016/j.cell.2018.09.013.
 基因君官网
基因君官网