在一项新的研究中,来自中国南京大学、南京工业大学和厦门大学的研究人员开发出利用病毒将CRISPR-Cas9基因编辑工具运送到特定细胞中的一种替代方法,它涉及使用两种类型的光。相关研究结果发表在2019年4月3日的Science Advances期刊上,论文标题为“Near-infrared upconversion–activated CRISPR-Cas9 system: A remote-controlled gene editing platform”。在这篇论文中,他们描述了他们的新型载体以及它在试验用小鼠中的效果。论文通讯作者为南京大学的宋玉君(Yujun Song)教授、南京工业大学的王玉珍(Yuzhen Wang)副研究员和厦门大学的林友辉(Youhui Lin)副教授。
CRISPR-Cas9基因编辑工具是治疗遗传疾病的一场即将到来的革命,科学家们继续在各种应用中测试它的能力。鉴于当前的方法使用病毒将这种基因编辑工具递送到特定细胞中,一个研究领域涉及寻找它的替代载体系统。人们较早地就已知道这种病毒递送方法不可行,这是因为免疫系统可能会做出反应,或者更糟的是,这存在着触发肿瘤产生的风险。在这项新的研究中,中国研究人员提出了一种全新的方法:利用两种光来递送这种基因编辑工具。
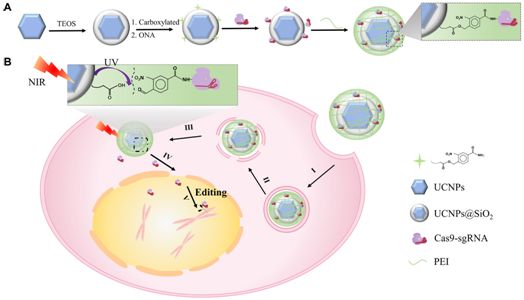
他们的载体系统由对低能近红外辐射(NIR)敏感并发出紫外光的上转换纳米颗粒(upconversion nanoparticle, UCNP)组成。当近红外光照射在这些上转换纳米颗粒上时,这种光被吸收并转换成紫外光,所产生的紫外光会发射出去。
在细胞内部,这种载体系统可通过给皮肤照射近红外光加以激活。照射的近红外光穿过皮肤进入体内,并前去寻找这种载体系统。当近红外光被上转换纳米颗粒转化为紫外光时,它切割这种载体系统中的分子,从而释放出这种基因编辑工具来完成它的作用。
在实际的实验中,这些研究人员通过注射将CRISPR-Cas9工具直接递送至小鼠内部的癌性肿瘤中。当它安全就位时,他们将近红外光照射到位于肿瘤(和基因编辑工具)所在部位上方的皮肤上。当所产生的紫外光释放出这种基因编辑工具时,它开始编辑一种允许肿瘤生长的蛋白,最终结果就是肿瘤尺寸减小。
这些研究人员表示,他们的研究不仅表明一种基于光的载体能够与CRISPR-Cas9基因编辑一起发挥作用,而且还表明它能够安全地发挥作用并且提供直接的益处。
参考资料:
Yongchun Pan et al. Near-infrared upconversion–activated CRISPR-Cas9 system: A remote-controlled gene editing platform, Science Advances (2019). DOI: 10.1126/sciadv.aav7199.
 基因君官网
基因君官网